Предмет: Химия,
автор: sashaa628473
1. Напишіть формулу вищого оксиду елемента, розміщеного в ѴІ групі 3 періоду Періодичної таблиці, обчисліть масову частку Оксигену в цьому оксиді, укажіть характер вищого оксиду, підтвердіть його написанням відповідних рівнянь реакції.
2. Назвіть елемент ѴІІ групи Періодичної таблиці, якщо масова частка Оксигену в його вищому оксиді становить 61,2%.
3. Елемент Е утворює летку сполуку з Гідрогеном складу Н2Е, у якій масова частка йо-го становить 97,53%. Укажіть відносну формульну масу його вищого оксиду.
ХТО НАПИШЕ БРЕТ ОТРИМАЄ БАН!!!!!!!!
ПРИКЛАД НАПИСАННЯ
Приложения:

Ответы
Автор ответа:
2
Ответ:
1 завдання на фото.
2 завдання)Т.к. элемент находится в 7 группе, то его высший
оксид -- Е207. Массовая доля элемента находится по формуле:
w(O) = Ar(O)*n/Mr(E207)
0,612 = 16°7/Mr(E207)
Mr(E207) = 112/0,612 = 183
Mr(E207) = 2"Ar(E) + 7'Ar(O)
183=2*Ar(E) + 112
2"Ar(E) = 71
Ar() = 35,5 => искомый элемент СІ (хлор).
3 завдання)Знаходимо відсоток водню: 100%-97,53%=2,47%
складаємо пропорцію
2--
--2,47%
X--
--97,53%
x=2*97,53/2,47=79
Це селен
оксид:::::ЅеОЗ Mr(SeO3)=79+16*3=127
Приложения:
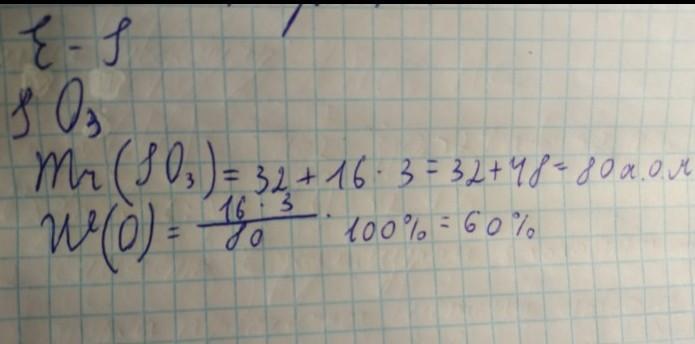
sashaa628473:
Дякую
що значить 2--
Похожие вопросы
Предмет: Математика,
автор: Аноним
Предмет: Литература,
автор: ram1k27
Предмет: Математика,
автор: arzamascevai34
Предмет: Химия,
автор: nastenilol
Предмет: Алгебра,
автор: 4444zs