Предмет: Химия,
автор: yanchik105
Расставьте степени окисления всех химических элементов, запишите
электронный баланс, расставьте коэффициенты, определите окислитель и
восстановитель – FeS + O2 = Fe2O3 + SO2.
Ответы
Автор ответа:
0
1) 4FeS2 (восс-ль) 11O2 (ок-ль) = 2Fe2O3 + 8SO2
окисление:2Fe+2 -6e- = 2Fe+34S-1 -20e- = 4S+4
2FeS2 -26e- = Fe2O3 + 4SO2 | 26 | 52 | 2 |
восстан-е:O2 +4e- = 2O2- | 4 | | 13 | - несмотря на правильность подсчетов, коэфф-т перед O2 нужно ставить 11, а не 13;
окисление:2Fe+2 -6e- = 2Fe+34S-1 -20e- = 4S+4
2FeS2 -26e- = Fe2O3 + 4SO2 | 26 | 52 | 2 |
восстан-е:O2 +4e- = 2O2- | 4 | | 13 | - несмотря на правильность подсчетов, коэфф-т перед O2 нужно ставить 11, а не 13;
Приложения:
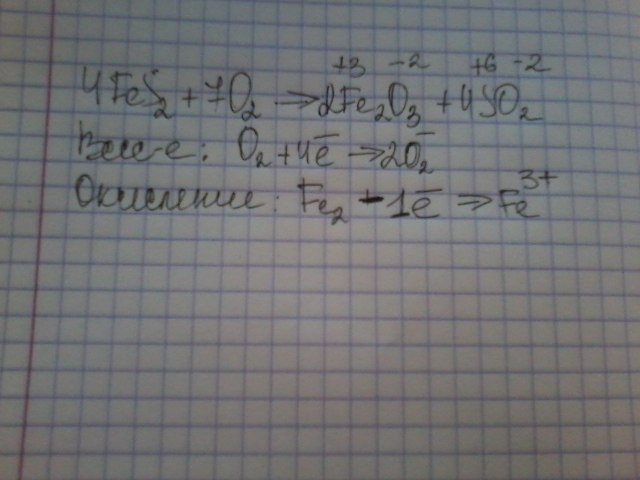
Автор ответа:
0
да
Автор ответа:
0
мне так и писать как написали?
Автор ответа:
0
спасибо вам большое
Похожие вопросы
Предмет: История,
автор: Аноним
Предмет: Русский язык,
автор: fireking20062006
Предмет: Математика,
автор: Jessicau
Предмет: Физика,
автор: 96sasha96