Предмет: Химия,
автор: vitaliybaiiika
Для элемента задана электронная формула внешнего слоя : 3d^6 4s^2
1.Определите, какой это элемент. Напишите его полную электрон-ную формулу. Укажите электронное семейство.
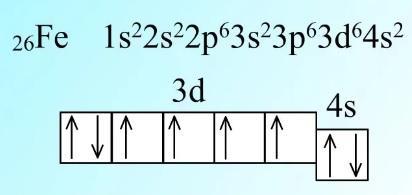
2. Расположите валентные электроны по энергетическим ячейкам. Укажите квантовые числа валентных электронов и валентность эле-мента в невозбужденном и возбужденном состояниях.
3. Охарактеризуйте окислительно-восстановительные свойства это-го элемента.
4. Определите высшую и низшую степени окисления элемента и приведите примеры соединений, в которых элемент проявляет эти сте-пени окисления.
5. Составьте электронные формулы для элемента в высшей и низ-шей степенях окисления и охарактеризуйте окислительно-восстанови-тельные свойства элемента в этих степенях окисления.
6. Охарактеризуйте химические свойства элемента, записав фор-мулы его оксидов, гидроксидов, гидридов. С помощью уравнений реакций подтвердите химический характер оксидов и гидроксидов элемента.
7. Покажите, как изменяются свойства элементов периода, в кото-ром находится ваш элемент.
8. Запишите элементы-аналоги и отметьте, как изменяются свойст-ва аналогов с увеличением номера периода.
Ответы
Автор ответа:
0
Ответ:
Напишу сколько успею за ограниченное время ответа.
1. Это Fe. Полная электронная формула
Fe 1s²2s²2p⁶3s²3p⁶4s²3d⁶ это d-металл
2. См. рисунок
3. Его свойства зависят от степени окисления. Так Fe⁺² может отдавать электроны - восстановитель. А Fe⁺³ может отдать 1 электрон - окислитель.
4. Высшая степень окисления +6 в ферратах (например K₂FeO₄), низшая +2 - соединение FeO
Объяснение:
Приложения:
Похожие вопросы
Предмет: Алгебра,
автор: ssmilk746
Предмет: Математика,
автор: lizagolovasenko37
Предмет: Українська мова,
автор: irbovna
Предмет: Математика,
автор: VIAD06