Предмет: Химия,
автор: ministrely1
Смесь магниевых и медных опилок массой 1,5 г. обработали избытком соляной кислоты. А результате реакции выделялся водород объемом 560 мл. (н.у.) Определить массовую долю меди в смеси.
Ответ:60%
Приложения:
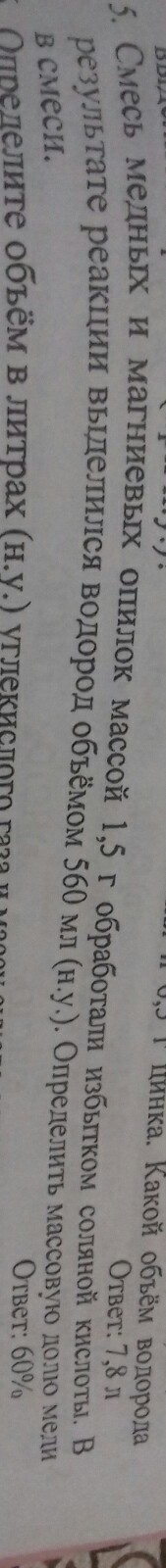
Ответы
Автор ответа:
0
Из этих металлов только магний реагирует с соляной кислотой.
Mg + 2 HCl = MgCl2 + H2 газ
n(H2)=V/Vm= 0.56/22.4=0.025 моль
n(Mg)=n(H2)=0.025 моль
m(Mg)= n•M= 0.025•24=0.6 грамм
m(Cu)=1.5-0.6=0.9 г
W(Cu) = (m (Cu)•100)/m смеси= (0.9•100)/1.6=60%
Mg + 2 HCl = MgCl2 + H2 газ
n(H2)=V/Vm= 0.56/22.4=0.025 моль
n(Mg)=n(H2)=0.025 моль
m(Mg)= n•M= 0.025•24=0.6 грамм
m(Cu)=1.5-0.6=0.9 г
W(Cu) = (m (Cu)•100)/m смеси= (0.9•100)/1.6=60%
Похожие вопросы
Предмет: Русский язык,
автор: gamzaevartur3
Предмет: Қазақ тiлi,
автор: daadiya9
Предмет: Английский язык,
автор: darhanesymhan
Предмет: Математика,
автор: Аничь1
Предмет: Обществознание,
автор: какая4