Предмет: Химия,
автор: sofiyaserysheva
1. Вычислите количество вещества оксида магния, необходимого для реакции с азотной кислотой, количеством 0,15 моль.
2. Вычислите массу рассчитанного в задаче №1 количества оксида магния.
Ответы
Автор ответа:
0
вот) задача лёгкая)даже очень)
Приложения:
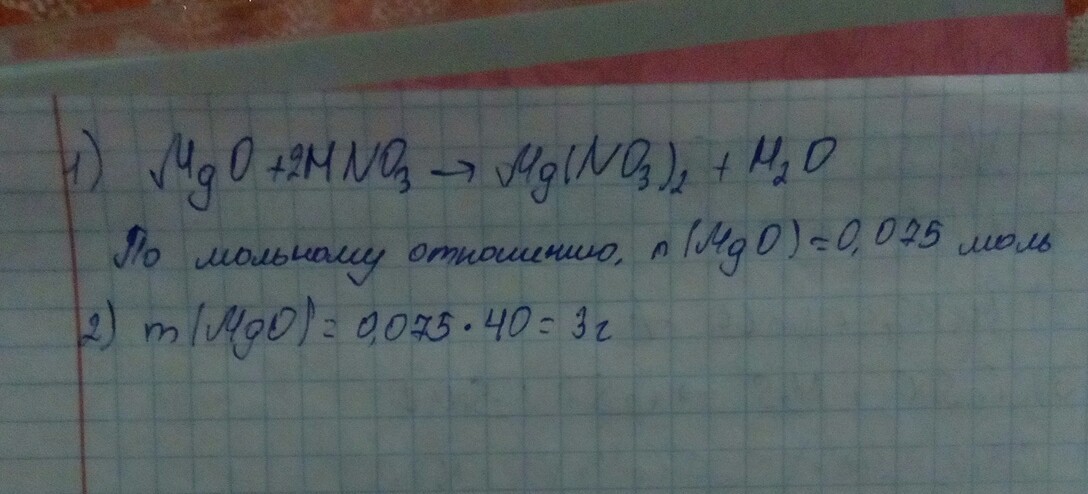
Автор ответа:
0
Дано:
n(HNO3) = 0.15 моль
Найти:
1. n(MgO)=?
2. m(MgO)=?
MgO + 2HNO3 = Mg(NO3)2 + H2O
Из УХР следует, что 1. n(MgO) = 1/2n(HNO3) = 0.5*0.15 моль =0,075 моль
2. M(MgO) = 40 г/моль
m(MgO) = 0.075 моль*40 г/моль =3 г
Ответ: 0,075 моль; 3 г MgO
n(HNO3) = 0.15 моль
Найти:
1. n(MgO)=?
2. m(MgO)=?
MgO + 2HNO3 = Mg(NO3)2 + H2O
Из УХР следует, что 1. n(MgO) = 1/2n(HNO3) = 0.5*0.15 моль =0,075 моль
2. M(MgO) = 40 г/моль
m(MgO) = 0.075 моль*40 г/моль =3 г
Ответ: 0,075 моль; 3 г MgO
Приложения:
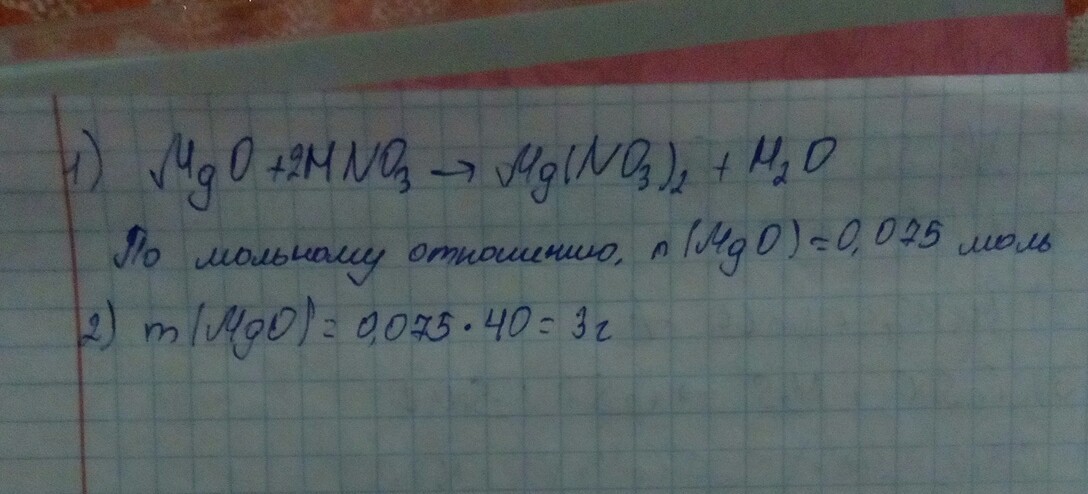
Похожие вопросы
Предмет: Химия,
автор: Аноним
Предмет: Химия,
автор: seeedaaaaa
Предмет: Физика,
автор: aminaashirbekova
Предмет: Математика,
автор: лика38п
Предмет: Алгебра,
автор: DashaKovakenko