Предмет: Химия,
автор: bcrangaci100499
Вычисли объём газа (н.у), который выделяется при взаимодействии карбоната калия массой 10грамм и раствора , содержащего 18,25 г хлороводорода
Ответы
Автор ответа:
0
123123123123123123132123
Приложения:
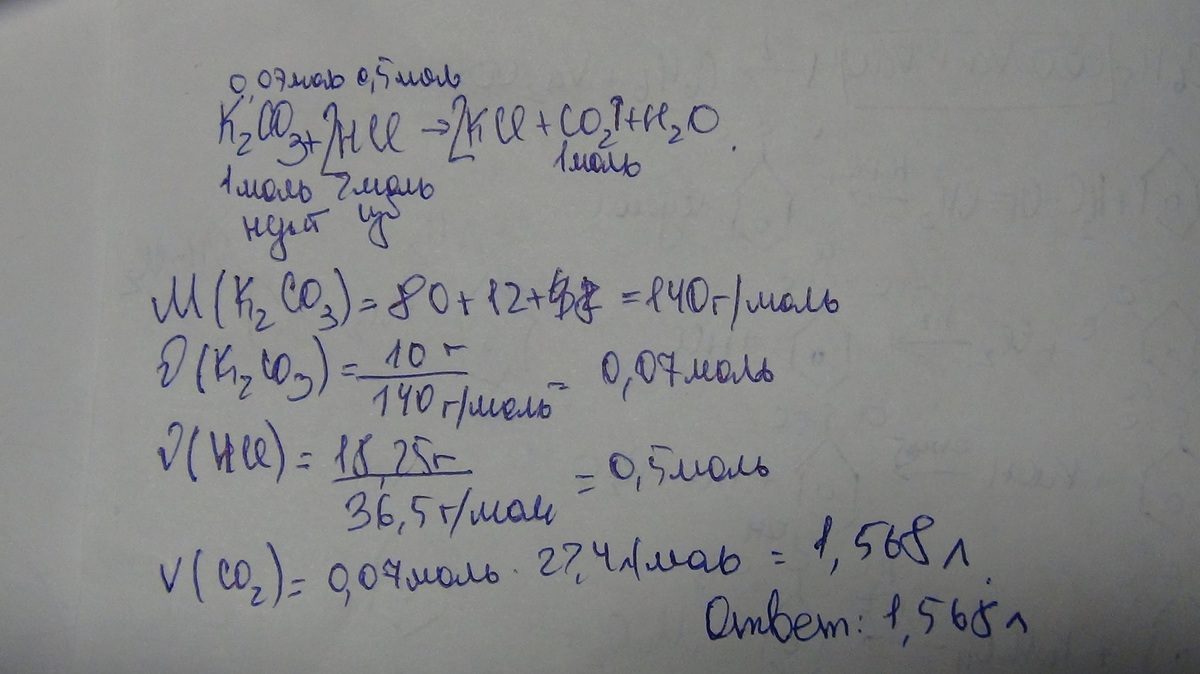
Аноним:
M(K2CO3)=2*39 + 12 + 3*16=78+12+48=138
Автор ответа:
1
K₂CO₃ + 2HCl = 2KCl + H₂O + CO₂↑
n(K₂CO₃)=10г \ 138г\моль=0,0725 моль
n(HCl)=18,25г \ 36,5г\моль = 0,5 моль
По уравнению реакции:
n(K₂CO₃):n(HCl)=1:2
K₂CO₃ в недостатке ⇒ расчёт ведём по нему
n(CO₂)=n(K₂CO₃)=0,0725 моль
V(CO₂)=0,0725 моль * 22,4 л\моль = 1,624 л ≈1,6л
Ответ: 1,6л
n(K₂CO₃)=10г \ 138г\моль=0,0725 моль
n(HCl)=18,25г \ 36,5г\моль = 0,5 моль
По уравнению реакции:
n(K₂CO₃):n(HCl)=1:2
K₂CO₃ в недостатке ⇒ расчёт ведём по нему
n(CO₂)=n(K₂CO₃)=0,0725 моль
V(CO₂)=0,0725 моль * 22,4 л\моль = 1,624 л ≈1,6л
Ответ: 1,6л
Похожие вопросы
Предмет: Русский язык,
автор: dashaturova25
Предмет: Русский язык,
автор: Ника2007р
Предмет: Русский язык,
автор: Адувалие
Предмет: Физика,
автор: recaptcha123
Предмет: Литература,
автор: Ivan16Belov