Предмет: Химия,
автор: leliiik15
составьте уравнение окислительно-восстановительных реакций и определите эквивалент восстановителя: KMnO4+H2S+H2SO4=MnSO4+K2SO4+H2O+S
Ответы
Автор ответа:
0
Реакция не совсем правильно записана. Поэтому она не будет уравнена.
Решение во вложении:
Решение во вложении:
Приложения:
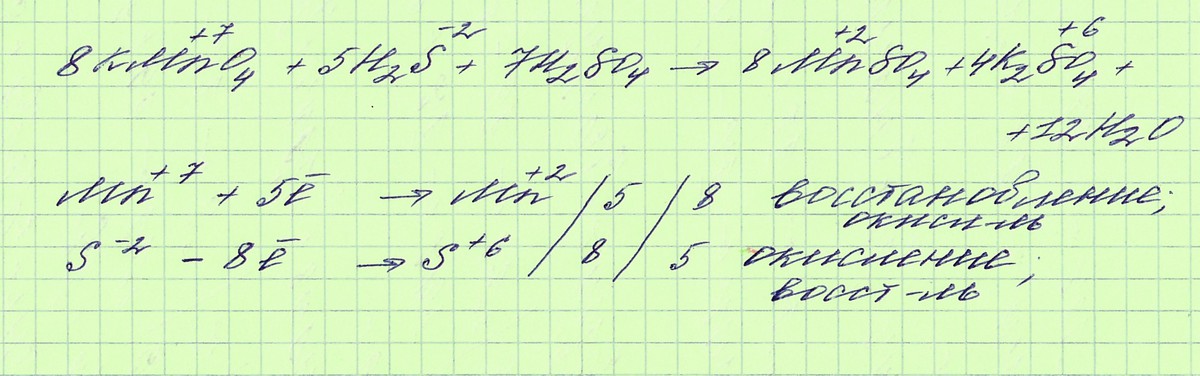
Автор ответа:
0
реакция может пойти по двум разным путям, в зависимости от соотношения реагентов
Автор ответа:
0
Ок ))) Вы правы )))
Автор ответа:
0
спасибо большое))
Автор ответа:
0
KMnO4 + H2S + H2SO4 = K2SO4 + MnSO4 + S + H2O
S2- - 2e = S0 процесс окисления - восстановитель
2KMnO4+5H2S+3H2SO4=5S+K2SO4+2MnSO4+8H2O
Mn(+7) +5e= Mn(+2) -2-в-ние; ок-ль
S(-2) -2e=S(0) -5-ок-ние;в-ль
2Mn(+7) + 5S(-2) = 2Mn(+2) + 5S(0)
эквивалент восстановителя = 1/2(эквивалент серы)
2KMnO4 + 5H2S + 3H2SO4 = 2MnSO4 + 5S + K2SO4 + 8H2O
S2- - 2e = S0 процесс окисления - восстановитель
2KMnO4+5H2S+3H2SO4=5S+K2SO4+2MnSO4+8H2O
Mn(+7) +5e= Mn(+2) -2-в-ние; ок-ль
S(-2) -2e=S(0) -5-ок-ние;в-ль
2Mn(+7) + 5S(-2) = 2Mn(+2) + 5S(0)
эквивалент восстановителя = 1/2(эквивалент серы)
Приложения:
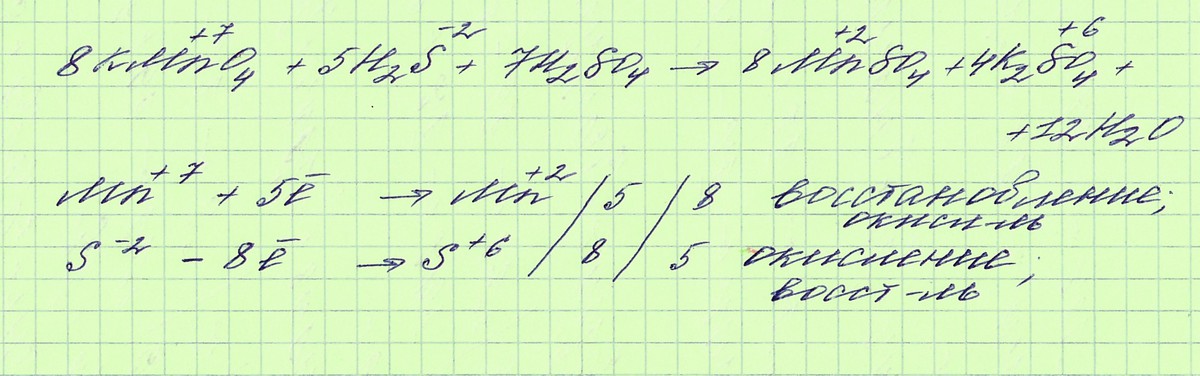
Автор ответа:
0
спасибо большое))
Автор ответа:
0
масса эквивалента серы=32/2=16 г/моль
Похожие вопросы
Предмет: Русский язык,
автор: karinakapenova
Предмет: Русский язык,
автор: nmusaeva54476
Предмет: Қазақ тiлi,
автор: Аноним
Предмет: Литература,
автор: sergeylider25
Предмет: История,
автор: yanburimenko