Предмет: Химия,
автор: Grant77
рассчитать массу сложного эфира, полученного при взаимодействии 30 г уксусной к-ты с избытком метанола, если массовая доля выхода продукта реакции составляет 60% от теоретического
Ответы
Автор ответа:
0
думаю что так) мне самой интересно :)
Приложения:
Автор ответа:
0
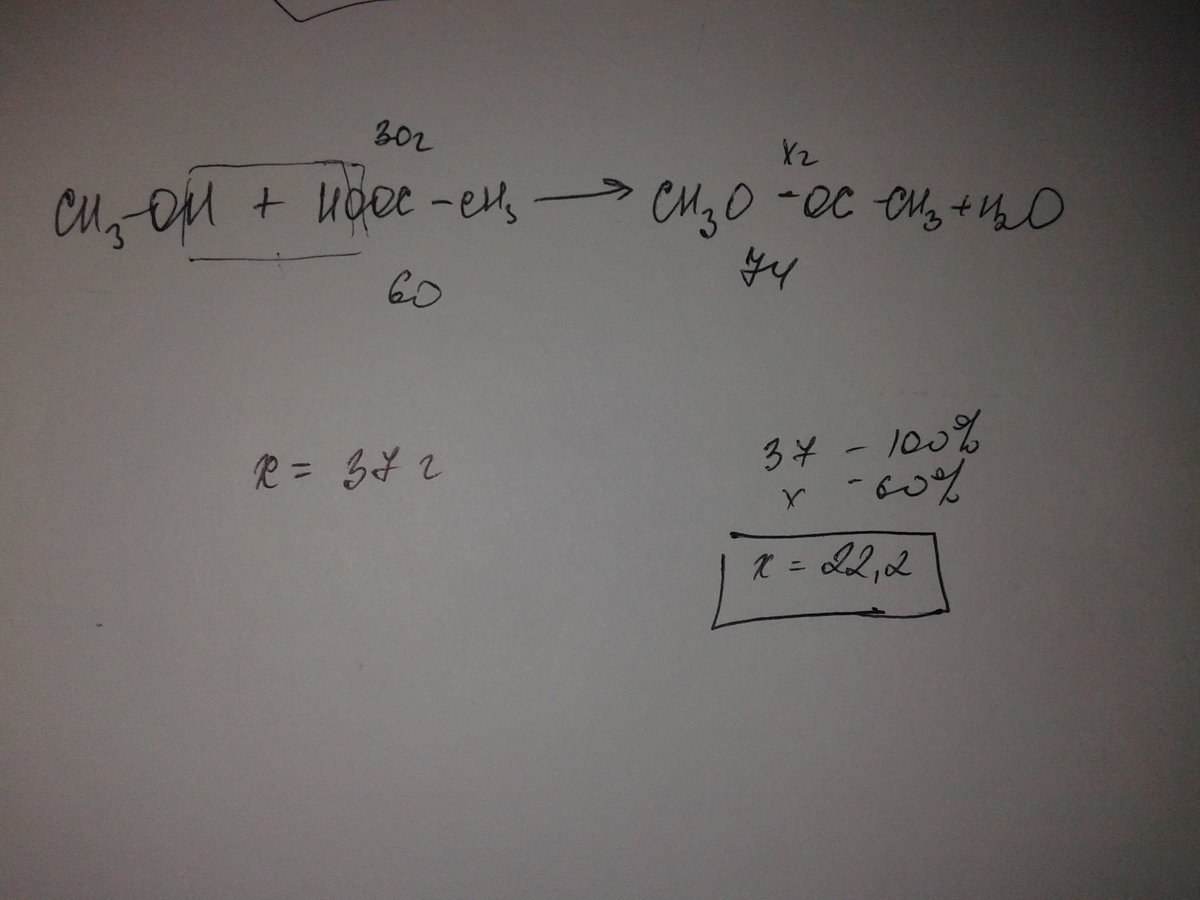
СH3COOH + CH3OH = CH3COOCH3 + H2O
над уксусной кислотой 30г. под уксусной кислотой 60г. над метилацетатом х, под метилацетатом 74, х по пропорции равен 37 г. - это масса теор.
Масса практ.=60%*37г./100%=22, 2 грамма
над уксусной кислотой 30г. под уксусной кислотой 60г. над метилацетатом х, под метилацетатом 74, х по пропорции равен 37 г. - это масса теор.
Масса практ.=60%*37г./100%=22, 2 грамма
Приложения:

Похожие вопросы
Предмет: Русский язык,
автор: Аноним
Предмет: Математика,
автор: ansarkarabalinov
Предмет: Математика,
автор: 1234567891aruzhan
Предмет: Информатика,
автор: lizabaSsi