Предмет: Химия,
автор: dasha471999
Помогите!Даю 30 баллов!
Найти массу гидроксида натрия который прореагировал с углекислым газом объёмом 4,48 л.
Ответы
Автор ответа:
0
Вот как то так получается.
Приложения:
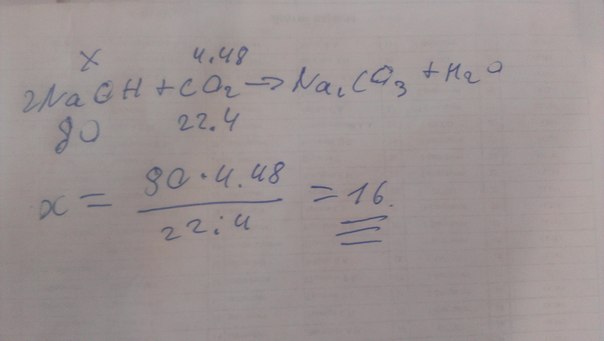
Автор ответа:
0
2NaOH+CO2=Na2CO3+H2O
ню(CO2)=22.4/4.48=5 моль
ню(NaOH)=5*2=10 моль
m(NaOH)=10*40=400 г
ню(CO2)=22.4/4.48=5 моль
ню(NaOH)=5*2=10 моль
m(NaOH)=10*40=400 г
Приложения:
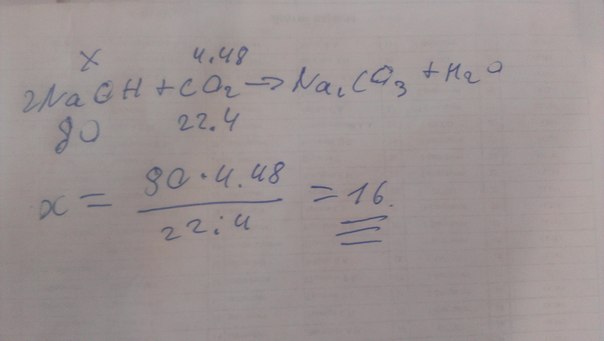
Автор ответа:
0
У тебя что то тут совсем не так, ню со2 0,2, атомную массу гидроксиди нужно умножить на два, так как стоит коэффицент 2 и т д....
Похожие вопросы
Предмет: История,
автор: strongvlada777
Предмет: Русский язык,
автор: xronenko65
Предмет: Русский язык,
автор: 51234557
Предмет: Информатика,
автор: YouirDoom