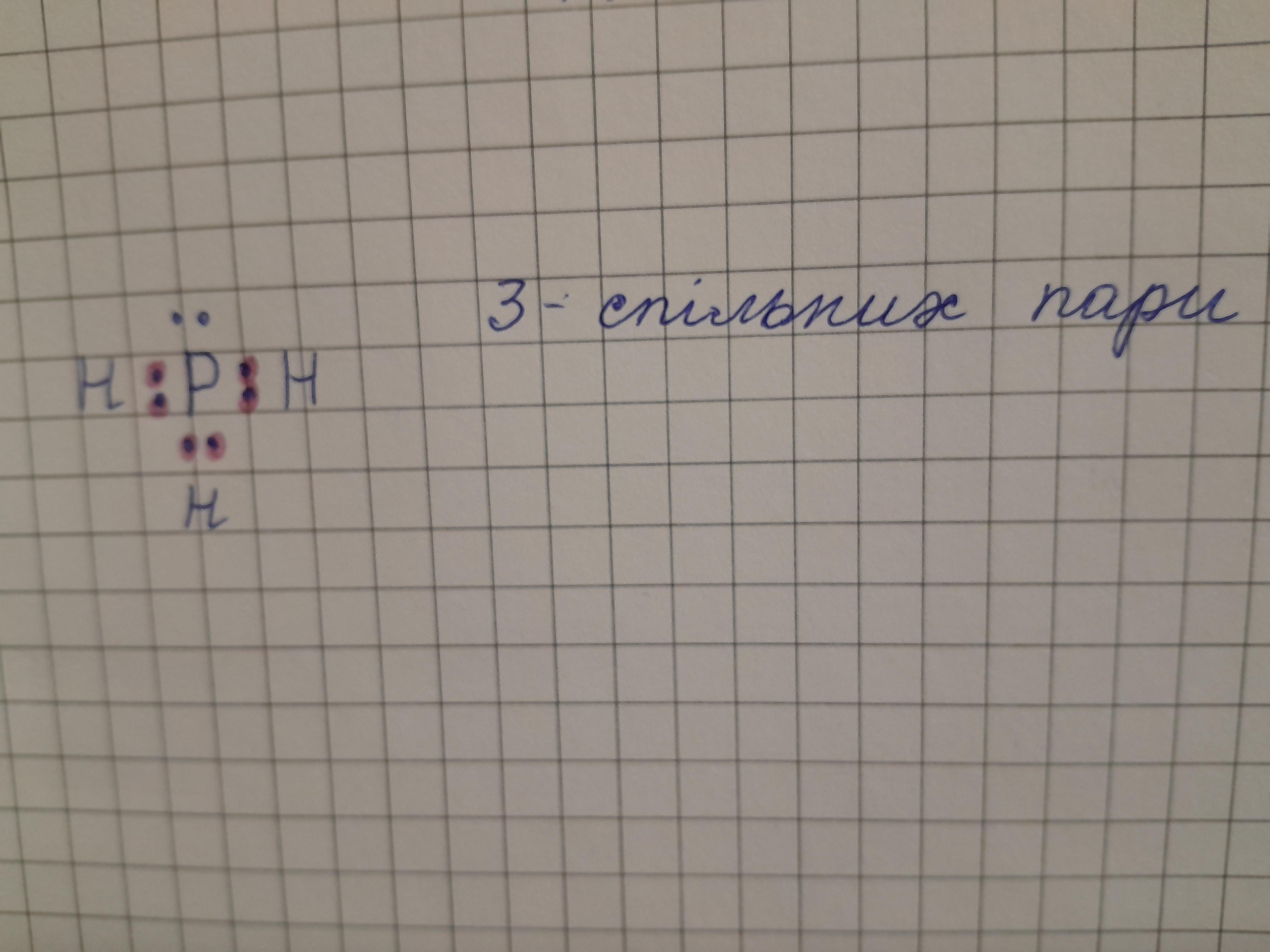ДАЮ 100 БАЛЛОВ!!! СРОЧНО!!!!
Завдання 4. Поясніть утворення хімічного звʼязку в РН3. Позначте утворення спільних електронних пар у молекулі.
Завдання 5. Елемент має на 4 електрони менше ніж йон Хлору. Вказати
елемент, дати йому характеристику.
Завдання 6. Елемент першої групи утворює оксид, відносна молекулярна
маса якого 94. Знайти елемент.
Ответы
Ответ:
Объяснение:
№4
РН3 - ковалентний полярний звʼязок
фото
№5
Йон Cl¹⁻ має 16 електронів
16 - 4 = 12
12 електронів має атом Магнію (Mg)
Магній міститься у 3 періоді, головній підгрупі II групи періодичної системи.
Відносна атомна маса Магнію Ar(Mg) = 24
Ядро атома Магнію містить 12 протонів. В атомі Магнію 12 електронів.
Число нейтронів у ядрі дорівнює різниці між нуклонним і протонним числом: 24 - 12 = 12.
Магній розміщуються на трьох енергетичних рівнях. В атомі Магнію перший і другий енергетичні рівні завершені. На зовнішньому енергетичному рівні є 2 валентні електрони.
Магній належить до s-елементів.
Магній належить до металічних елементів. Проста речовина магній метал. У сполуках Магній двовалентний.
№6
Формула вищого оксиду І групи Me₂O. Підставимо атомну масу Оксигену і молекулярну масу у формулу:
Me₂ + 16= 94
2Me = 94 - 16
2Me = 78
Me = 78 : 2
Me = 39
Цей елемент Калій його маса дорівніє 39