Заповніть ту таблицю по братськи
Ответы
Ответ:
Объяснение:
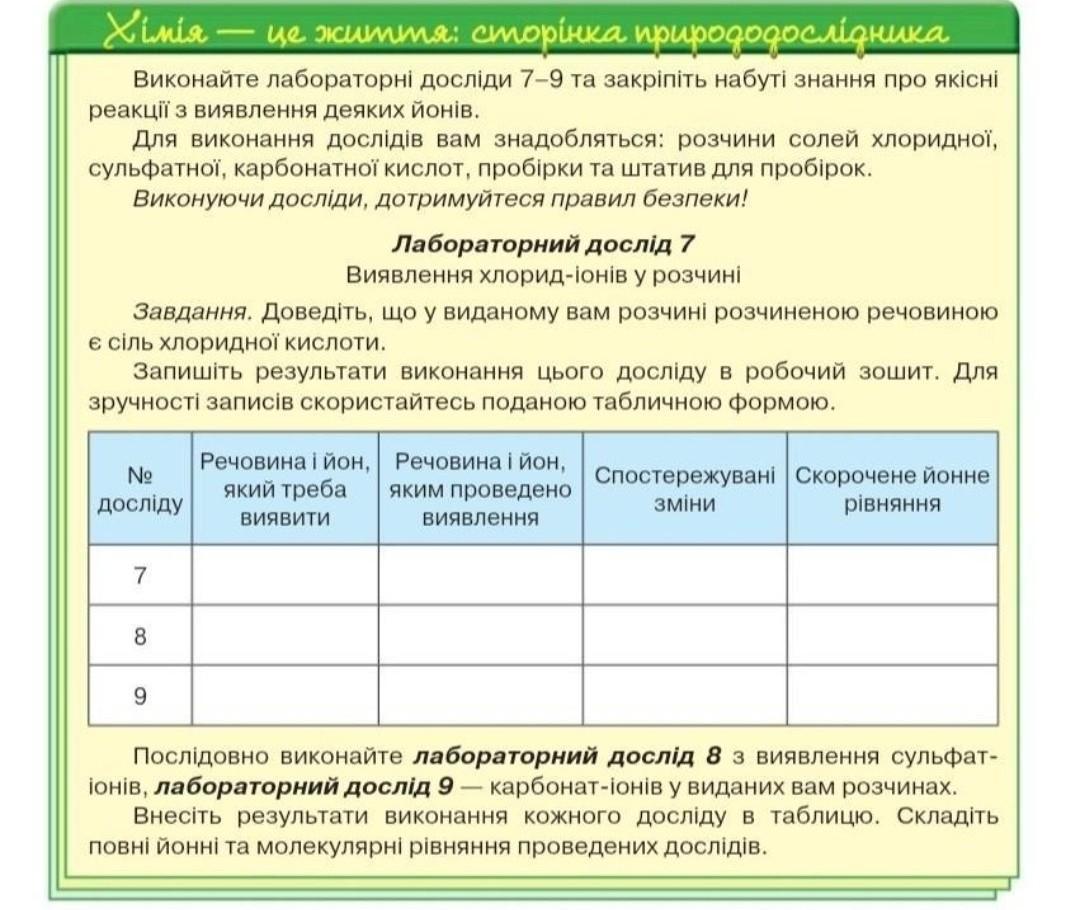
Дослід № 7
У першу пробірку наливаємо розчин натрій хлориду, у другу пробірку такий самий об'єм натрій нітрату, до обох пробірок додаємо розчин аргентум нітрату.
1. Речовина AgCl і йон Cl⁻ який треба виявити.
2. Речовина AgNO₃ і йон NO₃⁻ яким проведено виявлення.
3.Спостережувані зміни. Поява осаду у першій пробірці. Утворення білого сернистого осаду AgCl, що не розчиняється у нітратній кислоті , доводить те, що у пробіркі містяться хлорид - іони
NaCl + AgNO₃ = AgCl↓ + NaNO₃
Na⁺ + Cl⁻ + Ag⁺ + NO₃⁻ = AgCl↓ + Na⁺ + NO₃⁻
Ag⁺ + Cl⁻ = AgCl↓
Дослід № 8
У першу пробірку наливаємо розчин натрій хлориду, у другу пробірку такий самий об'єм натрій сульфату, до обох пробірок додаємо розчин барій хлориду.
1. Речовина BaSO₄ і йон SO₄²⁻ який треба виявити.
2. Речовина BaCl₂ і йон NO3 яким проведено виявлення.
3.Спостережувані зміни. Поява осаду у другій пробірці. Утворення білого дрібнокристалічного осаду BaSO₄, що не розчиняється кислотах , доводить те, що у пробіркі містяться сульфат - іони
Na₂SO₄ + BaCl₂ = 2NaCl + BaSO₄↓
2Na⁺ + SO₄²⁻ + Ba²⁺ + 2Cl⁻ = 2Na⁺ + 2Cl⁻ + BaSO₄↓
SO₄²⁻ + Ba²⁺ = BaSO₄↓
Дослід №9
1) У першу пробірку наливаємо розчин натрій хлориду, у другу пробірку такий самий об'єм натрій карбонату, до обох пробірок додаємо розчин кальцій хлориду.
1. Речовина CaCO₃ і йон CO₃²⁻ який треба виявити.
2. Речовина CaCl₂ і йон Cl⁻ яким проведено виявлення.
3.Спостережувані зміни. Поява осаду у другій пробірці. Утворення білого осаду CaCO₃,
Na₂CO₃ + CaCl₂ = CaCO₃↓ + 2NaCl
2Na⁺ + CO₃²⁻ + Ca²⁺ + 2Cl⁻ = 2Na⁺ + 2Cl⁻ + CaCO₃↓
Ca²⁺ + CO₃²⁻ = CaCO₃↓
2)У першу пробірку наливаємо розчин натрій нітрату, у другу пробірку такий самий об'єм натрій карбонату, до обох пробірок додаємо розчин хлоридної кислоти.
Спостерігаємо : виділення великої кількості газу.
Підносений до отвору пробірки запалений сірник перестає горіти і гасне.
Na₂CO₃ + 2HCl = 2NaCl + H₂O + CO₂↑
2Na⁺ + CO₃²⁻ + 2H⁺ + 2Cl⁻ = 2Na⁺ + 2Cl⁻ + H₂O + CO₂↑
2H⁺ + CO₃²⁻ = H₂O + CO₂↑