Предмет: Химия,
автор: melkey
Решите пожалуйста! Очень нужно!
Приложения:

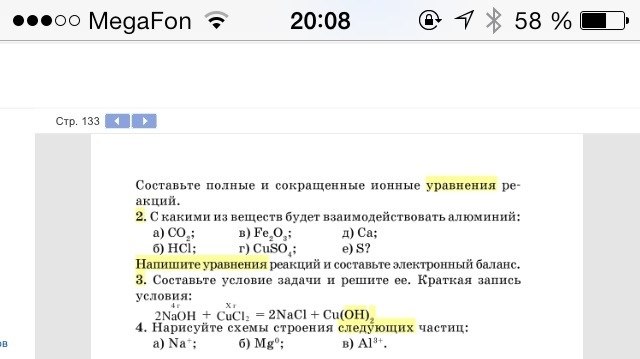
Ответы
Автор ответа:
0
цепочка:
1) CaO + CO2 = CaCO3
2) CaCO3 + CO2 + H2O = Ca(HCO3)2
3) Ca(HCO3)2 =(t°)= CaCO3 + CO2 + H2)
4) CaCO3 + 2HCl = CaCl2 + H2O + CO2
2Al + Fe2O3 = 2Fe + Al2O3
Al⁰ - 3e⁻ = Al⁺³ - окисление, Al⁰ - восстановитель
Fe⁺³ + 3e⁻ = Fe⁰ - восстановление, Fe⁺³- окислитель
2Al + 6HCl = 2Alcl3 + 3H2
Al⁰ - 3e⁻ Al⁺³, окисление, Al⁰-восстановитель
2H⁺ + 2e⁻ = H₂⁰, восстановление, H⁺ - окислитель
2Al + 3CuSO4 = Al2(SO4)3 + 3Cu
Al⁰ - 3e⁻ = Al⁺³, окисление, Al⁰ - восстановитель
Cu⁺² + 2e⁻ = Cu⁰, восстановление, Cu⁺² - окислитель
2NaOH + CuSO4 = Na2SO4 + Cu(OH)2
Условие: Какая масса сульфата меди(II) вступит в реакцию с 4 граммами едкого натра?
Решение:
Рассчитаем количество вещества гидроксида натрия:
n = m/M = 4г/40г/моль = 0,1 моль
По уравнению реакции:
n(CuSO4) = 1/2n(NaOH) = 0.05 моль
Рассчитаем массу сульфата меди(II):
m = n*M = 0,05моль*160 г/моль = 8 грамм.
Ответ: ...
1) CaO + CO2 = CaCO3
2) CaCO3 + CO2 + H2O = Ca(HCO3)2
3) Ca(HCO3)2 =(t°)= CaCO3 + CO2 + H2)
4) CaCO3 + 2HCl = CaCl2 + H2O + CO2
2Al + Fe2O3 = 2Fe + Al2O3
Al⁰ - 3e⁻ = Al⁺³ - окисление, Al⁰ - восстановитель
Fe⁺³ + 3e⁻ = Fe⁰ - восстановление, Fe⁺³- окислитель
2Al + 6HCl = 2Alcl3 + 3H2
Al⁰ - 3e⁻ Al⁺³, окисление, Al⁰-восстановитель
2H⁺ + 2e⁻ = H₂⁰, восстановление, H⁺ - окислитель
2Al + 3CuSO4 = Al2(SO4)3 + 3Cu
Al⁰ - 3e⁻ = Al⁺³, окисление, Al⁰ - восстановитель
Cu⁺² + 2e⁻ = Cu⁰, восстановление, Cu⁺² - окислитель
2NaOH + CuSO4 = Na2SO4 + Cu(OH)2
Условие: Какая масса сульфата меди(II) вступит в реакцию с 4 граммами едкого натра?
Решение:
Рассчитаем количество вещества гидроксида натрия:
n = m/M = 4г/40г/моль = 0,1 моль
По уравнению реакции:
n(CuSO4) = 1/2n(NaOH) = 0.05 моль
Рассчитаем массу сульфата меди(II):
m = n*M = 0,05моль*160 г/моль = 8 грамм.
Ответ: ...
Приложения:
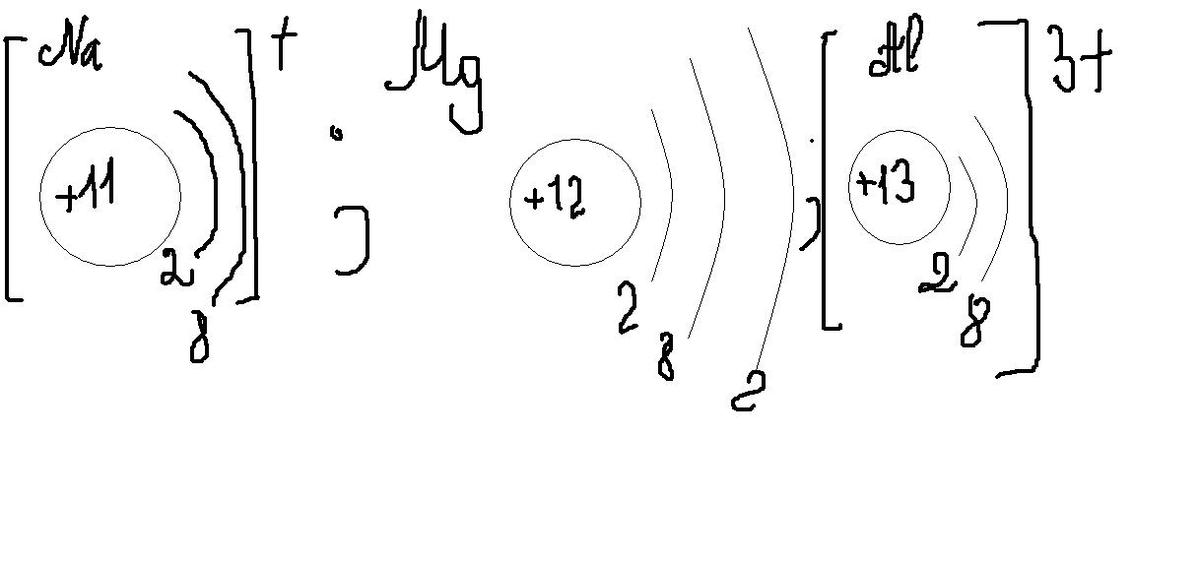
Похожие вопросы
Предмет: Қазақ тiлi,
автор: adilkansundet9
Предмет: Химия,
автор: evaalievna0
Предмет: История,
автор: ali4karomanova260419
Предмет: Биология,
автор: sanya099
Предмет: Математика,
автор: isakova19971