Предмет: Химия,
автор: vicushha
допоможіть будь ласка
Приложения:
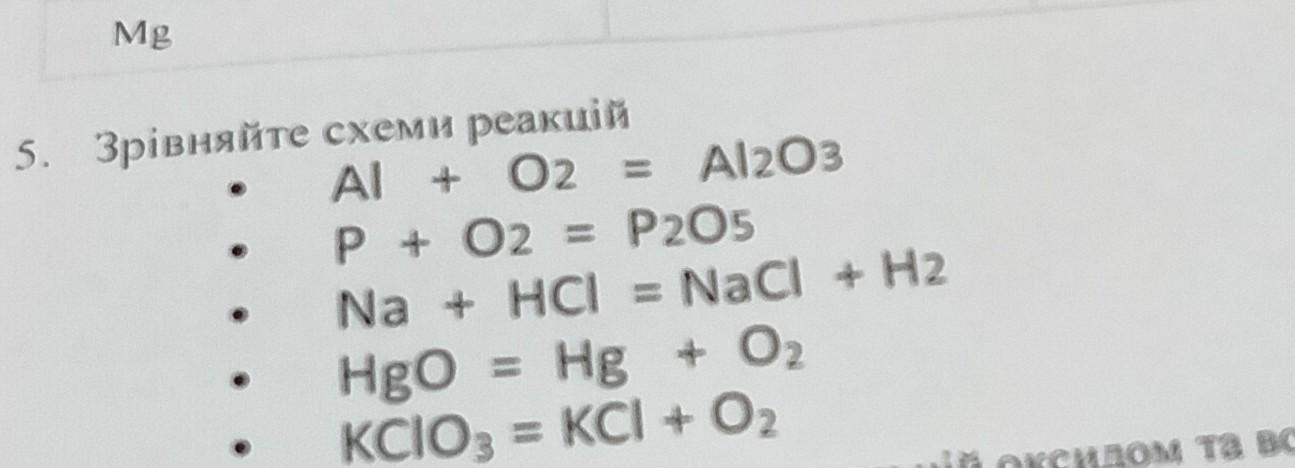
Ответы
Автор ответа:
1
1. 4 Al (s) + 3 O2 (g) → 2 Al2O3 (s)
Это окислительно-восстановительная (редокс) реакция:
4 Al0 - 12 e- → 4 AlIII
(окисление)
6 O0 + 12 e- → 6 O-II
(восстановле́ние)
2. 4 P + 5 O2 → 2 P2O5
Это окислительно-восстановительная (редокс) реакция:
4 P0 - 20 e- → 4 PV
(окисление)
10 O0 + 20 e- → 10 O-II
(восстановле́ние)
3. 2 Na + 2 HCI → 2 NaCI + H2
Это окислительно-восстановительная (редокс) реакция:
2 Na0 - 2 e- → 2 NaI
(окисление)
2 HI + 2 e- → 2 H0
(восстановле́ние)
4. 2 HgO (s) → 2 Hg (l) + O2 (g)
Это окислительно-восстановительная (редокс) реакция:
2 HgII + 4 e- → 2 Hg0
(восстановле́ние)
2 O-II - 4 e- → 2 O0
(окисление)
5. KClO3O3 → KCl + 3 O2
Это окислительно-восстановительная (редокс) реакция:
ClXI + 12 e- → Cl-I
(восстановле́ние)
6 O-II - 12 e- → 6 O0
(окисление)
Это окислительно-восстановительная (редокс) реакция:
4 Al0 - 12 e- → 4 AlIII
(окисление)
6 O0 + 12 e- → 6 O-II
(восстановле́ние)
2. 4 P + 5 O2 → 2 P2O5
Это окислительно-восстановительная (редокс) реакция:
4 P0 - 20 e- → 4 PV
(окисление)
10 O0 + 20 e- → 10 O-II
(восстановле́ние)
3. 2 Na + 2 HCI → 2 NaCI + H2
Это окислительно-восстановительная (редокс) реакция:
2 Na0 - 2 e- → 2 NaI
(окисление)
2 HI + 2 e- → 2 H0
(восстановле́ние)
4. 2 HgO (s) → 2 Hg (l) + O2 (g)
Это окислительно-восстановительная (редокс) реакция:
2 HgII + 4 e- → 2 Hg0
(восстановле́ние)
2 O-II - 4 e- → 2 O0
(окисление)
5. KClO3O3 → KCl + 3 O2
Это окислительно-восстановительная (редокс) реакция:
ClXI + 12 e- → Cl-I
(восстановле́ние)
6 O-II - 12 e- → 6 O0
(окисление)
Похожие вопросы
Предмет: Українська мова,
автор: Antroper
Предмет: Математика,
автор: popopopop26
Предмет: Музыка,
автор: Аноним
Предмет: Русский язык,
автор: supernat83