Предмет: Химия,
автор: Аноним
Сколько литров H2 выделится при взаимодействии 9 г Al с 200 мл 2М HCl?
Ответы
Автор ответа:
0
Удачи!!!!!!!!!!!!!!!!!!!!!!!!!
Приложения:

Автор ответа:
0
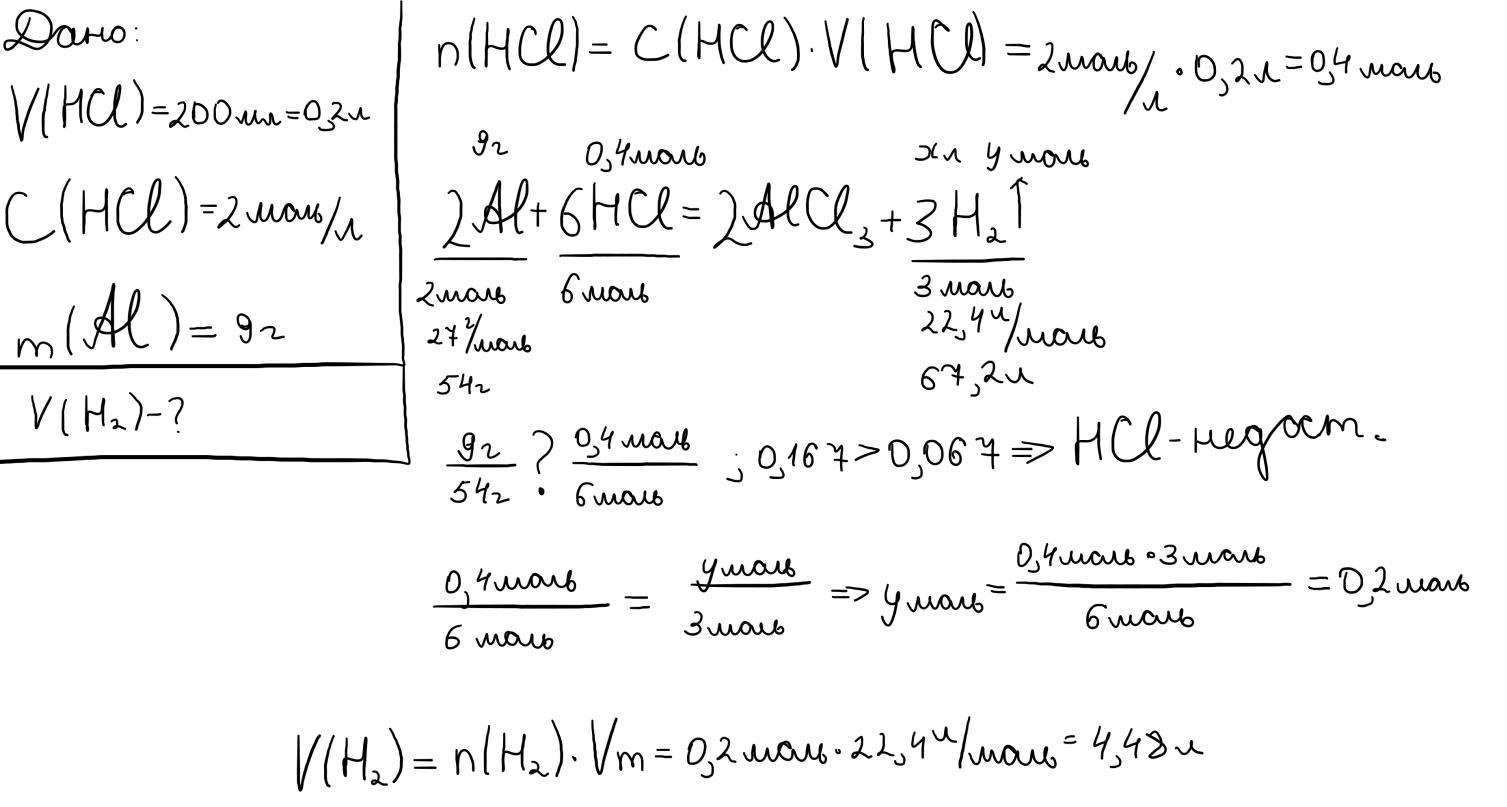
Дано:
m(Al) = 9 г
V р-ра(HCl) = 200 мл = 0,2 л
См(HCl) = 2 М
Найти:
V(H2) - ?
Решение:
1) 2Al + 6HCl → 2AlCl3 + 3H2;
2) n(Al) = m / M = 9 / 27 = 0,33 моль;
3) n(HCl) = См * V р-ра = 2 * 0,2 = 0,4 моль;
4) HCl в недостатке, расчеты по нему;
5) n(H2) = n(HCl) * 3 / 6 = 0,4 * 3 / 6 = 0,2 моль;
6) V(H2) = n(H2) * Vm = 0,2 * 22,4 = 4,48 л.
Ответ: Объем H2 составляет 4,48 л.
Похожие вопросы
Предмет: География,
автор: yliaostapenko08
Предмет: Геометрия,
автор: davidnehoda282
Предмет: Физика,
автор: handusenkokirill9
Предмет: Право,
автор: mildil02
Предмет: Русский язык,
автор: deman1234678