вычислите массу хлорида кальция полученного из 175 граммов карбоната кальция содержащего 10% примесей?
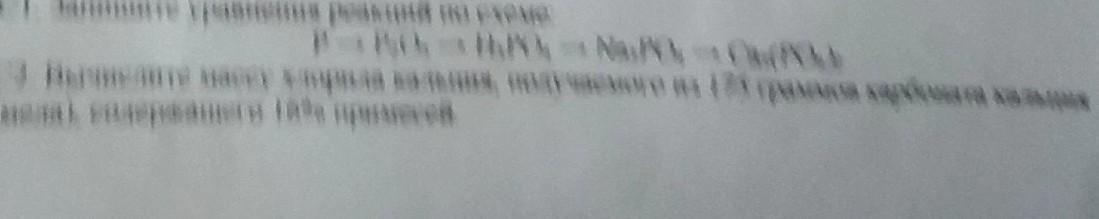
Ответы
Ответ:
87,3 г
Объяснение:
Масса чистого карбоната кальция в 175 граммах с учетом 10% примесей будет:
175 г * (1 - 0,1) = 157,5 г
Молярная масса CaCO₃ (карбоната кальция) равна 100,1 г/моль, а молярная масса CaCl₂ (хлорида кальция) равна 110,98 г/моль.
Чтобы вычислить массу хлорида кальция, полученного из 157,5 г карбоната кальция, нужно сначала перевести массу карбоната кальция в количество вещества в молях, затем использовать коэффициенты стехиометрии, чтобы найти количество вещества хлорида кальция, а затем перевести количество вещества в массу хлорида кальция.
Количество вещества карбоната кальция:
n = m/M = 157,5 г / 100,1 г/моль = 1,574 моль
Количество вещества хлорида кальция, получаемого из карбоната кальция, равно количеству вещества карбоната кальция, умноженному на коэффициент стехиометрии между CaCO₃ и CaCl₂, который равен 1/2:
n(CaCl₂) = n(CaCO₃) * 1/2 = 1,574 моль * 1/2 = 0,787 моль
Масса хлорида кальция:
m(CaCl₂) = n(CaCl₂) * M(CaCl₂) = 0,787 моль * 110,98 г/моль = 87,3 г
Таким образом, масса хлорида кальция, полученного из 175 г карбоната кальция, содержащего 10% примесей, составляет 87,3 г.
Відповідь:87,3 г
Пояснення:
n(CaCl₂) = n(CaCO₃) * 1/2 = 1,574 моль * 1/2 = 0,787 моль
Масса хлорида кальция:
m(CaCl₂) = n(CaCl₂) * M(CaCl₂) = 0,787 моль * 110,98 г/моль = 87,3 г