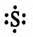6 Складiть формулу Льюїса для молекули сірки S2. Скільки електронних
пар беруть участь в утворенні ковалентного зв'язку між атомами Суль-
фуру? Чи виконується правило октету?
9*. Складіть графічні електронні формули для електронних оболонок
атомів Фосфору та Хлору в основному та різних можливих збуджених
станах. Ґрунтуючись на них, поясніть можливі валентності, що можуть
виявляти атоми Фосфору та Хлору в сполуках
Ответы
Ответ:
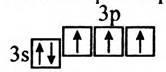
Сульфур. Елекгронна оболонка складається з трьох енергетичних рівнів. На зовнішньому енергетичному рівні містяться дві пари електронів і два неспарені електрони. Електронна формула: 1s22s22p63s23p3. Будова зовнішнього електронного рівня: (фото 043)
Формула Льюїса: ( фото 044)
У молекулі сірки S2 в утворенні ковалентного зв’язку беруть участь дві пари електронів. Правило октету виконується: (053)
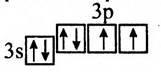
Фосфор. Електронна оболонка складається з трьох енергетичних рівнів. На зовнішньому енергетичному рівні міститься пара електронів і три неспарені електрони. Електронна Формула: 1s22s22p63s23p3. Будова зовнішнього електронного рівня: (045)
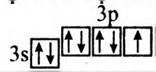
Хлор. Електронна оболонка складається з трьох енергетичних рівнів. На зовнішньому енергетичному рівні містяться три пари електронів і один неспарений електрон. Електронна формула: 1s22s12p63s23p5. Будова зовнішнього електронного рівня: (041)
ad
Объяснение: