Практическая работа "Получение соляной кислоты и изучение ее свойств"
Ответы
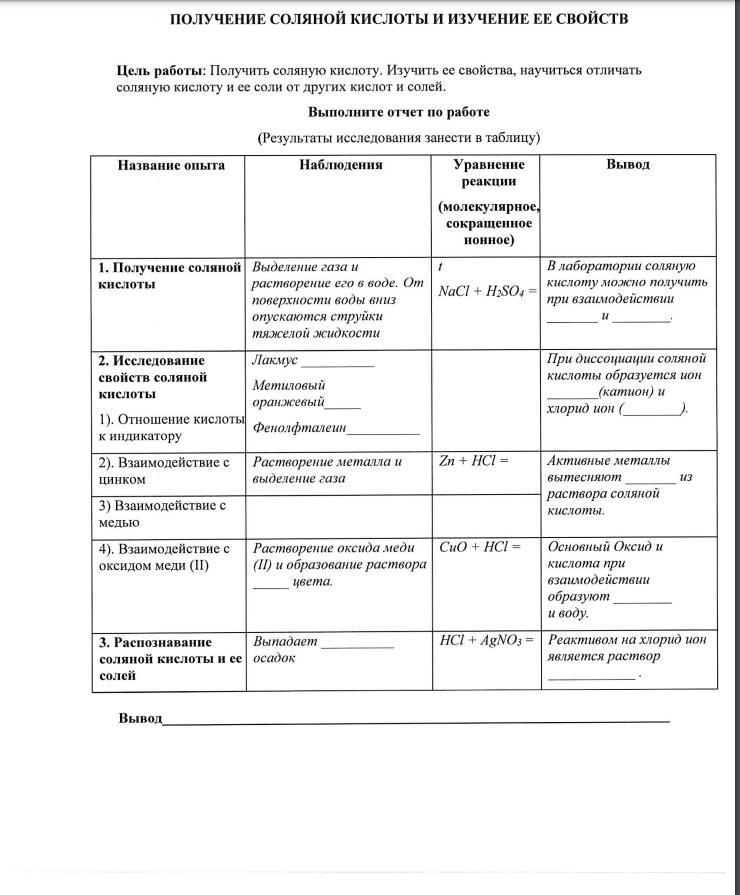
1) В лаборатории соляную кислоту получают при взаимодействии хлорида натрия и серной кислоты. 2NaCl + H2SO4 → Na2SO4 + 2HCl
2) Действие с индикаторами:
Лакмус становится красным
Метилоранж становится розовым
Фенолфталеин не меняет цвет, т.е. остается бесцветным
Диссоциация одноступенчатая:
HCl → H + Cl
H+ катион, Cl- анион.
Реакция цинка с соляной кислотой:
Zn + 2HCl → ZnCl2 + H2↑
(цинк вытесняет водород из соляной кислоты)
Cu + HCl → реакция не происходит, потому что медь не может вытеснить водород.
А вот с оксидом меди (II) реакция происходит:
CuO + 2HCl → CuCl2 + H2O
Происходит образование соли - хлорида меди (II), голубовато-зеленого цвета.
3) При реакции HCl + AgNO3 → AgCl + HNO3
Выпадает осадок, белого цвета - AgCl (хлорид серебра).
Вывод - Соляная кислота, или хлороводородная кислота - сильная одноосновная кислота.
H2 + Cl2 → 2HCl↑ - это газ хлороводород, который в промышленности растворяют в воде, получая соляную кислоту.