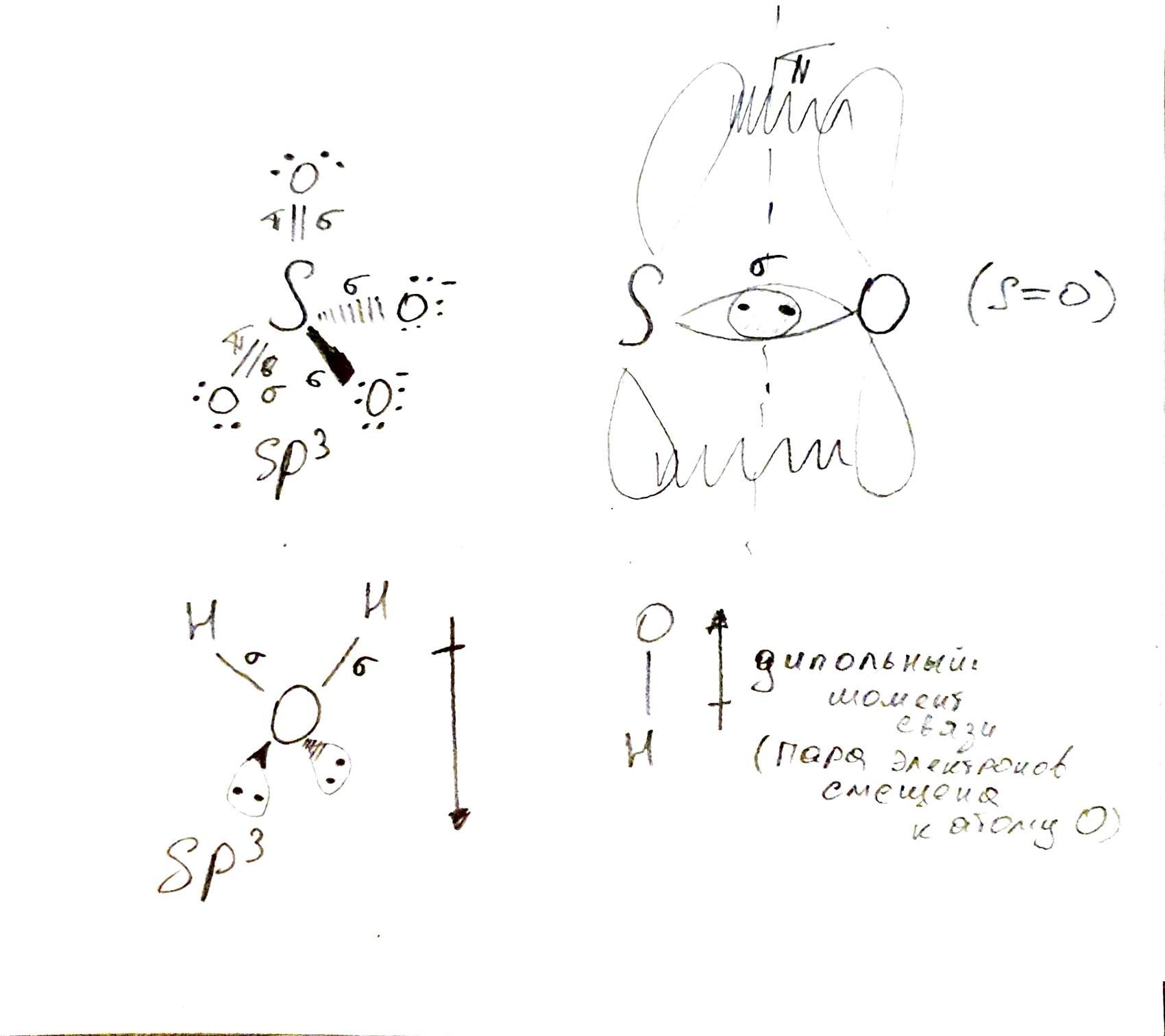
Опишите строение частиц H2О, SO4−2 методом валентных связей: тип гибридизации АО серы и кислорода, число и тип связей, геометрическую форму и угол между связями. Локализованные или делокализованные -связи в этих частицах? Полярна ли молекула H2О (дайте обоснованный ответ)?
Ответы
Ответ:
Ион имеет форму правильного тетраэдра (рис 1), поэтому все углы в связях практически равны значению в 109.5 градусов.
Атом серы имеет гибридизацию .
Сера соединена с отрицательно заряженными атомами кислорода связью проходящей через линию (рис 3) между связеобразующими атомами, поэтому это σ (сигма связь)
С нейтрально заряженными атомами кислорода образуется одна σ и одна π, так как p орбитали пересекаются перпендикулярно линии связи. Итого 4 сигма и 2 пи связи.
Пи связи в молекуле сульфат иона делокализированы, так как охватывают более 2 атомов
Молекула воды имеет две связи, обе типа σ (сигма), так как орбитали образуют связь проходящую через линию между атомами (O-H)
Молекула формы тетраэдра (рис 2) и имеет дипольный момент (то есть она полярна), так как каждая из O-H связей имеет свой дипольный момент направленный в сторону атома кислорода, которые вместе дают избыточный положительный заряд δ⁺ со стороны атомов водорода и избыточный отрицательный δ⁻ у атома кислорода.
Угол связи H-O-H несколько меньше 109.5 градусов, типичных для sp³ гибридизации из-за взаимного отталкивания электронных пар кислорода и связей.
Атом кислорода sp³ гибридизации