Предмет: Химия,
автор: kotikvaru
Помогите, пожалуйста . Как это делать?
Приложения:


Ответы
Автор ответа:
1
Это реакции ОВР(окислительно-восстановительные реакции), то есть меняется степень окисления двух атомов; в образце это алюминий и кислород.
При помощи ОВР уравнивают реакции по следующему алгоритму:
1) Расставляют степени окисления у всех атомов(с опытом уже видно, какие атомы поменяли степень окисления, поэтому подписывают только их)
2) Под реакцией слева записывают атом с исходной степенью окисления, потом идёт стрелочка, а справа записывают атом с конечной степенью окисления, со вторым атомом делают тоже самое.
3) Далее считают сколько атом отдал или принял электронов. Например: заряд был 0, а стал +3, следовательно атом ОТДАЛ 3 электрона, то есть -3е. Электрон имеет отрицательный заряд, поэтому если мы прибавляем электрон - заряд понижается; а если отнимаем - повышается(как минус на минус даёт плюс)
4) Находим число, которое делится на число электронов в первой строчке и во второй.(как в математике при сложении дробей мы ищем общий знаменатель)
5) Далее делим это число(которое только что нашли) на число электронов в первой строчке - это будет наш коэффициент, тоже самое делаем со второй строчкой.
6) Коэффициенты, которые мы получили, ставятся перед всеми веществами, содержащие этот атом.
Решение здания будет на фото, надеюсь, мои объяснения помогут Вам понять эту тему. Поставьте, пожалуйста, лайк и оцените мой ответ))
Ещё комментарий по поводу реакций из задания. В первой реакции скорее всего образуется FeBr3, так как бром сильный окислитель. Вторая реакция вообще не существует, так как молекула брома это Br2, но никак не Br3; к тому же железо крайне редко проявляет степень окисления +6 и в школьном курсе это не рассматривается. Четвёртой реакции тоже не существует, неорганические соли никогда не взаимодействуют с водоводом.
При помощи ОВР уравнивают реакции по следующему алгоритму:
1) Расставляют степени окисления у всех атомов(с опытом уже видно, какие атомы поменяли степень окисления, поэтому подписывают только их)
2) Под реакцией слева записывают атом с исходной степенью окисления, потом идёт стрелочка, а справа записывают атом с конечной степенью окисления, со вторым атомом делают тоже самое.
3) Далее считают сколько атом отдал или принял электронов. Например: заряд был 0, а стал +3, следовательно атом ОТДАЛ 3 электрона, то есть -3е. Электрон имеет отрицательный заряд, поэтому если мы прибавляем электрон - заряд понижается; а если отнимаем - повышается(как минус на минус даёт плюс)
4) Находим число, которое делится на число электронов в первой строчке и во второй.(как в математике при сложении дробей мы ищем общий знаменатель)
5) Далее делим это число(которое только что нашли) на число электронов в первой строчке - это будет наш коэффициент, тоже самое делаем со второй строчкой.
6) Коэффициенты, которые мы получили, ставятся перед всеми веществами, содержащие этот атом.
Решение здания будет на фото, надеюсь, мои объяснения помогут Вам понять эту тему. Поставьте, пожалуйста, лайк и оцените мой ответ))
Ещё комментарий по поводу реакций из задания. В первой реакции скорее всего образуется FeBr3, так как бром сильный окислитель. Вторая реакция вообще не существует, так как молекула брома это Br2, но никак не Br3; к тому же железо крайне редко проявляет степень окисления +6 и в школьном курсе это не рассматривается. Четвёртой реакции тоже не существует, неорганические соли никогда не взаимодействуют с водоводом.
Приложения:
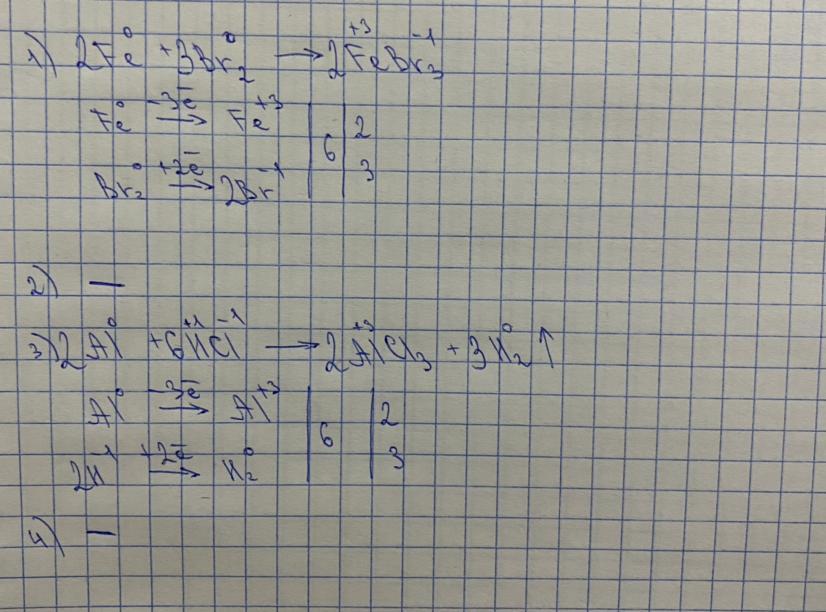
Похожие вопросы
Предмет: Українська мова,
автор: anyusya7
Предмет: Русский язык,
автор: коу3
Предмет: Русский язык,
автор: Мишарулит
Предмет: Алгебра,
автор: babahumawp
Предмет: Математика,
автор: chexova73