Предмет: Математика,
автор: khalimovaelina986
Сделайте пожалуйста
Приложения:
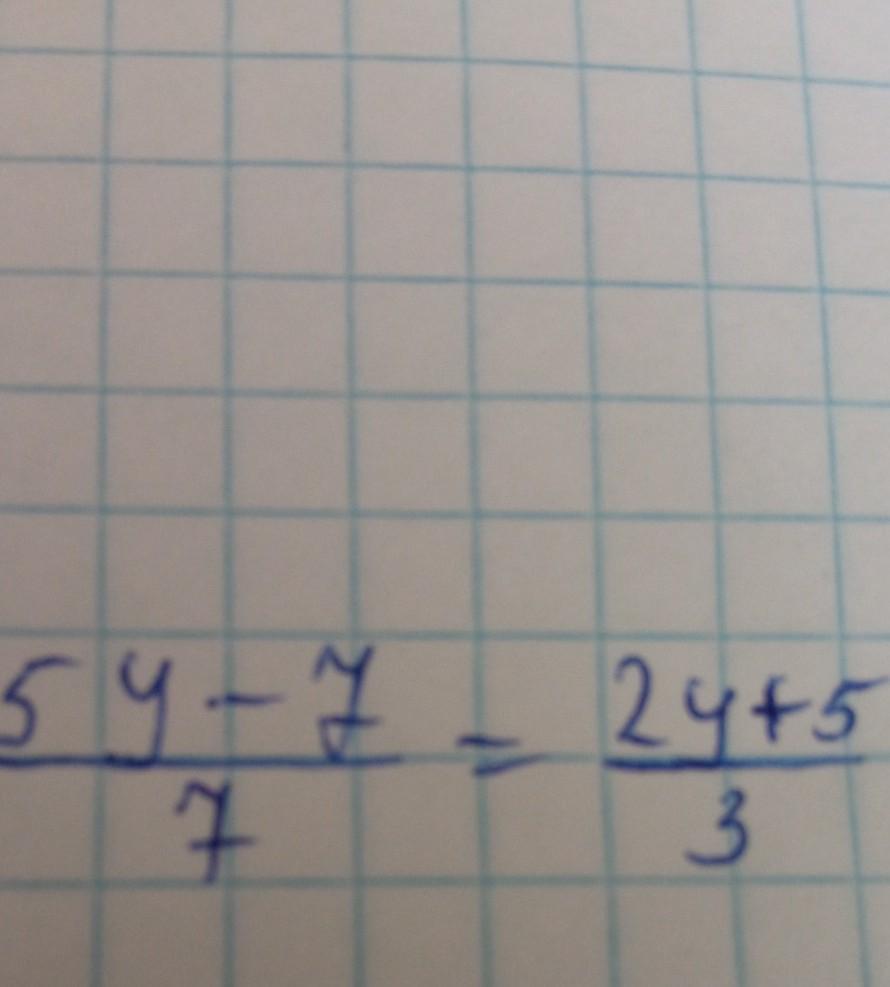
fawafwfaf:
после 5 это y?
Ответы
Автор ответа:
2
Відповідь:
y=56
Покрокове пояснення:
5y-7/7=2y+5/3 (умножаем на 21 для уничтоженния дробей)
3(5y-7)=7(2y+5)
15y-21=14y+35
15y-14y=35+21
y=56
Автор ответа:
2
Пошаговое объяснение:
(5у - 7)/7 = (2у + 5)/3
7 * (2у + 5) = 3 * (5у - 7)
14у + 35 = 15у - 21
14у - 15у = -21 - 35
-у = -56
у = 56
Похожие вопросы
Предмет: Русский язык,
автор: FFFFGGGG55
Предмет: Английский язык,
автор: 1SadMeow1
Предмет: Русский язык,
автор: anjasimonyan
Предмет: Химия,
автор: Хле6ушек
Предмет: Биология,
автор: sjosipivba