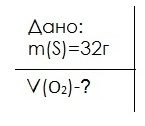Какой объем кислорода потребуется для сжигания 32 г серы
Ответы
мварщшкпщкугпх щуктгпх9угпху9гпхф90угп хтфгпхфухпеуыхфпа
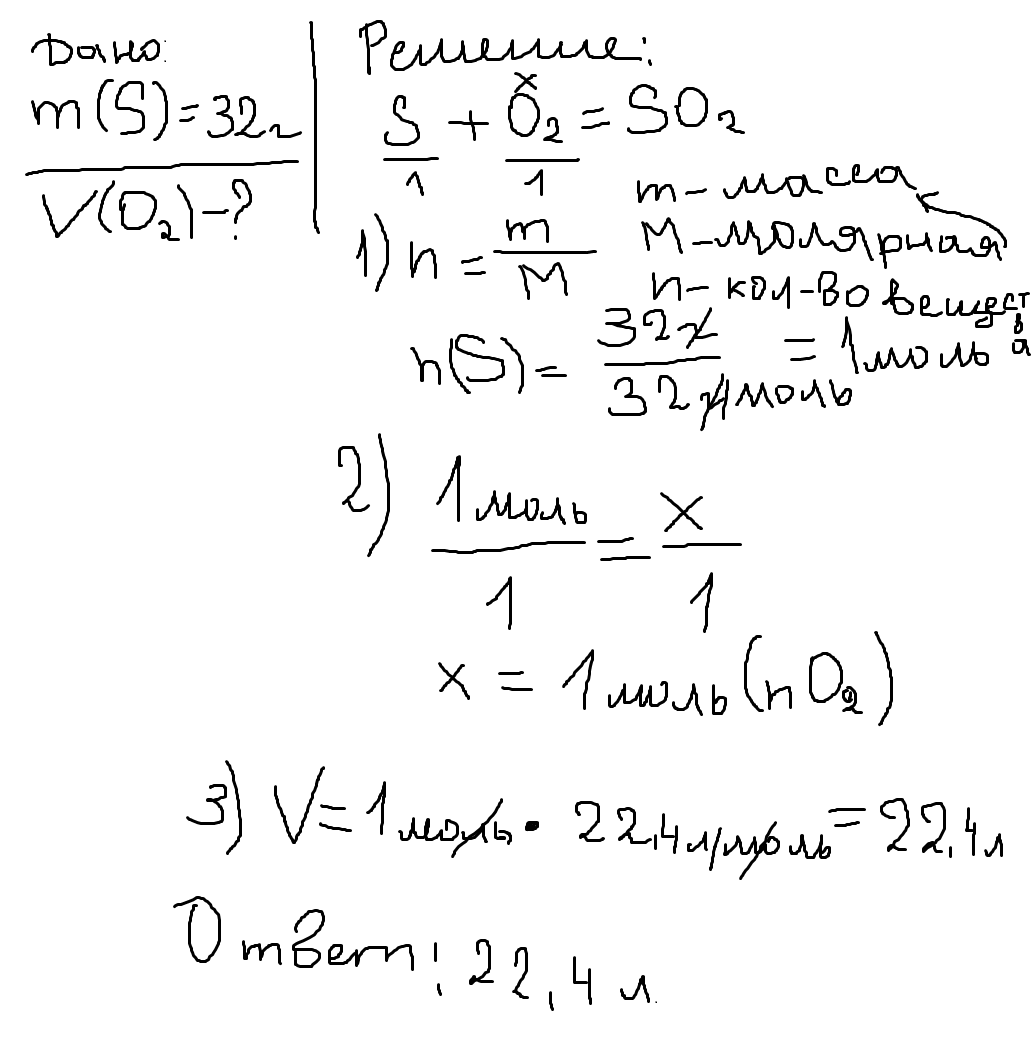
Решение
S+O₂-->SO₂
Сначала нужно найти колличество серы по формуле , где n-колличество вещества, m-масса, M-молярная масса (её находят, пользуясь таблицей Мегделеева).
n(S)=32г:32г/моль=1моль
Теперь смотрим на коэффициенты перед серой и кислородом. Т. к. перед ними нет никаких цифр, значит, коэффициент перед сарой 1, а перед кислородом тоже 1. Следовательно колличество кислорода равно колличеству серы.
n(O₂)=n(S)=1моль
Теперь можем найти объём кислорода по формуле: , где
V-объём, n-колличество, - молярный объём (у газов он всегда равен 22,4 л/моль).
V(O₂)=1моль·22,4л/моль=22,4 л
Ответ: 22,4 л.
Если нужно, то "Дано" во вложении: