Химия 8 класс, ИУ 35неделя!!!
50 баллов!!!!!
1. Определи валентность элемента в его соединении с водородом НІ.
Ответ запиши римской цифрой. Например: IV.
Ответ: валентность иода равна….
2. Найдите валентность железа в его соединение с кислородом,формула соединения — Fe2O3
ответ запишите римской цифрой например: IV
ответ: валентности железо равнa…
3. Выбери химический элемент высшая валентность которого равна V
ответ: Свенсен, Астат, фосфор, Молибден
4. Расположи формуле в порядке увеличения валентность и хлора:
1) HCl 2)CI2O3 3)CI2O5 4)Cl2O7
5. Отметь символы химических элементов которые в соединениях проявляются только положительные степень окисления:
Mn
H
F
Br
Mg
6. Запиши максимальное значение степени степени окисления для марганца.
ответ запиши, пример, так: 5+
ответ: …
7. Укажи минимальное значение степени окисления для серы.
ответ запиши, например, так: -4
ответ: …
8. Определи степень окисления элементов оксида Br2O3
Ответ запишите так же как и в задании 7/6
Ответ: …
Ответы
Ответ:
1.Валентность йода - I
2. Валентность железа - III
3. Фосфор (P)
4. Они уже расположены по порядку
5. Mn, Mg.
6. +7
7. -2
8. +3 - бром, - 2 - кислород.
Объяснение:
1. Т.к у водорода постоянная вал. = 1, а при йоде не стоит коэффицент(подразумевается 1), то вал. йода в данном соединении равна 1.
2. У кислорода постоянная вал. = 2, у железа же она чаще всего 3, либо 4. Так ты берешь и находишь НОК двух коэфф. = 3х2 =6. Дальше делишь на его на коэфф. который стоит при элементе - 6/2=3 - вал. Fe - 3.
3. Высшая вал. смотрится по группе. В VА группе из вышеперечисленного присутствует только фосфор.
4. Смотри пункт 2.
5. Только положительную степень окисления принимают металлы.
6.Смотри пункт 3.
7. Тут все вообще просто, от номера группы отнимаешь 8.
Сера в VIА гр. 6-8= -2.
8. У кислорода постоянная степень окисления = -2. Далее умножаешь коэфф. на степень, получается при кислороде стоит 3. Зх(-2)= -6. Далее смотришь на коэфф. при другом элементе(бром), и подбираешь степень окисления так, чтобы в итоге выйти в ноль. В данном случае 2х3= 6. 6+(-6)=0. Готово))
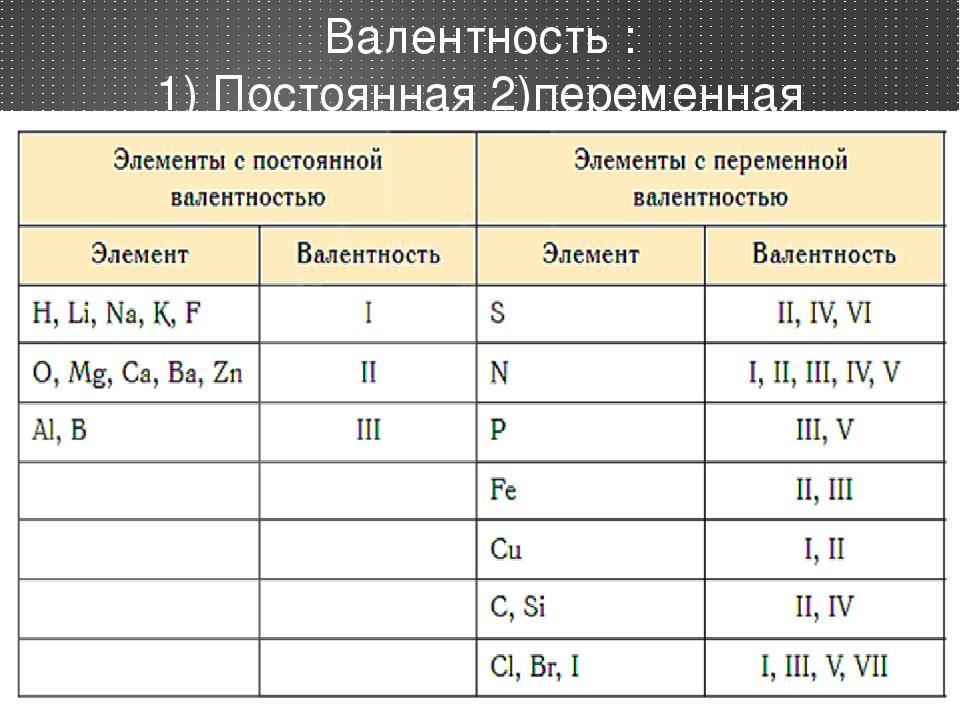
Однако есть элементы у которых постоянная валентность и степень окисления, это уже придётся выучить ...
Высшая степень окисления совпадает с номером группы элемента (для элементов в главной подгруппе) в короткой форме периодической системы.
Низшая степень окисления равна числу, которое получится, если от номера группы элемента отнять 8.
Исключения: фтор, железо, кобальт, родий, подгруппа никеля, кислород, благородные газы (помимо ксенона).
Всегда пожалуйста)