Предмет: Химия,
автор: MazikinMaze
Методом электронно-ионных уравнений составьте полные уравнения реакций, учитывая, что либо окислитель, либо восстановитель являются также и средой. Обоснуйте на основании стандартных окислительно-восстановительных потенциалов возможность протекания данных реакций.
Приложения:
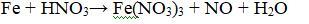
Ответы
Автор ответа:
1
Решение:
Fe + HNO₃ → Fe(NO₃)₃ + NO + H₂O
Fe + H⁺ + NO₃⁻ → Fe⁺³ + 3NO₃⁻ + NO + H₂O
анод катод
Fe - 3e⁻ → Fe⁺³ | 3 | | 1 | - восстановитель
| | 3 | |
NO₃⁻ + 4H⁺ + 3e⁻ → NO + 2H₂O | 3 | | 1 | - окислитель
------------------------------------------------------------------------------------------------
Fe - 3e⁻ + NO₃⁻ + 4H⁺ + 3e⁻ → Fe⁺³ + NO + 2H₂O
Fe + NO₃⁻ + 4H⁺ → Fe⁺³ + NO + 2H₂O
Fe + 4NO₃⁻ + 4H⁺ → Fe⁺³ + 3NO₃⁻ + NO + 2H₂O
Fe + 4HNO₃ → Fe(NO₃)₃ + NO↑ + 2H₂O
Решено от :
MazikinMaze:
спасибо большое!
помогите с заданием, пожалуйста!
https://znanija.com/task/48881849
https://znanija.com/task/48881849
Похожие вопросы
Предмет: Қазақ тiлi,
автор: raul3klass
Предмет: Русский язык,
автор: dimkazorlayng
Предмет: Қазақ тiлi,
автор: stanislav190620
Предмет: География,
автор: Ttaga
Предмет: Экономика,
автор: orbusik747