Предмет: Химия,
автор: wismur2000
1. Запишите уравнения реакций перехода. Для первого перехода (1-й реакции) составить электронный баланс (ЭБ), в последней реакции (5) составить ионное уравнение.
C -> AL4C3 -> CH4 -> CO2 -> Na2 CO3 -> CaCO3
2. Напишите в молекулярном и кратком ионном виде уравнения реакций распознавания солей: сульфата калия (K2SO4) и силиката калия (K2SiO3). Что наблюдается в ходе реакций?
3. Составить электронный баланс, расставить коэффициенты для следующей реакции:
Hg + HNO3 (конц) -> Hg (NO3)2 + NO2 + H2O
4. Найти массу железа, вступившего в реакцию замещения с 200 граммами 9,8%-ного раствора серной кислоты?
5. Рассчитайте содержание питательного элемента в следующих солях: фосфате аммония (NH4)3PO4 и карбонате калия (K2CO3) ?
Ответы
Автор ответа:
1
Ответ: 1) 4 Al + 3 C → Al4C3.
C(0) + 4e → C(-4) восстановление.
Al(0) - 3e → Al(+3) окисление.
2) Al4C3 + 12 H2O → 4 Al(OH)3 + 3 CH4.
3) CH4 + 2 O2 → 2 H2O + CO2.
4) 2 NaOH + CO2 → H2O + Na2CO3.
5) CaCl2 + Na2CO3 → 2 NaCl + CaCO3.
Ca(2+) + 2Cl(-) + 2Na(+) + CO3(2-) → 2Na(+) + 2Cl(-) + CaCO3.
Ca(2+) + CO3(2-) → CaCO3.
1) K2SO4 + BaCl2 → 2 KCl + BaSO4 (белый осадок).
Ba(2+) + SO4(2-) → BaSO4.
2) K2SiO3 + 2 HCl → 2 KCl + H2SiO3 (желеобразный осадок).
SiO3(2-) + 2H(+) → H2SiO3.
3) Hg + 4 HNO3 → 2 H2O + Hg(NO3)2 + 2 NO2.
Hg(0) - 2e → Hg(+2) окисление.
N(+5) + 1e → N(+4) восстановление.
4 во вложении.
5) W(N) = 14*3/149 * 100% = 28,19%.
W(K) = 39*2/138 * 100% = 56,52%.
Объяснение:
Приложения:
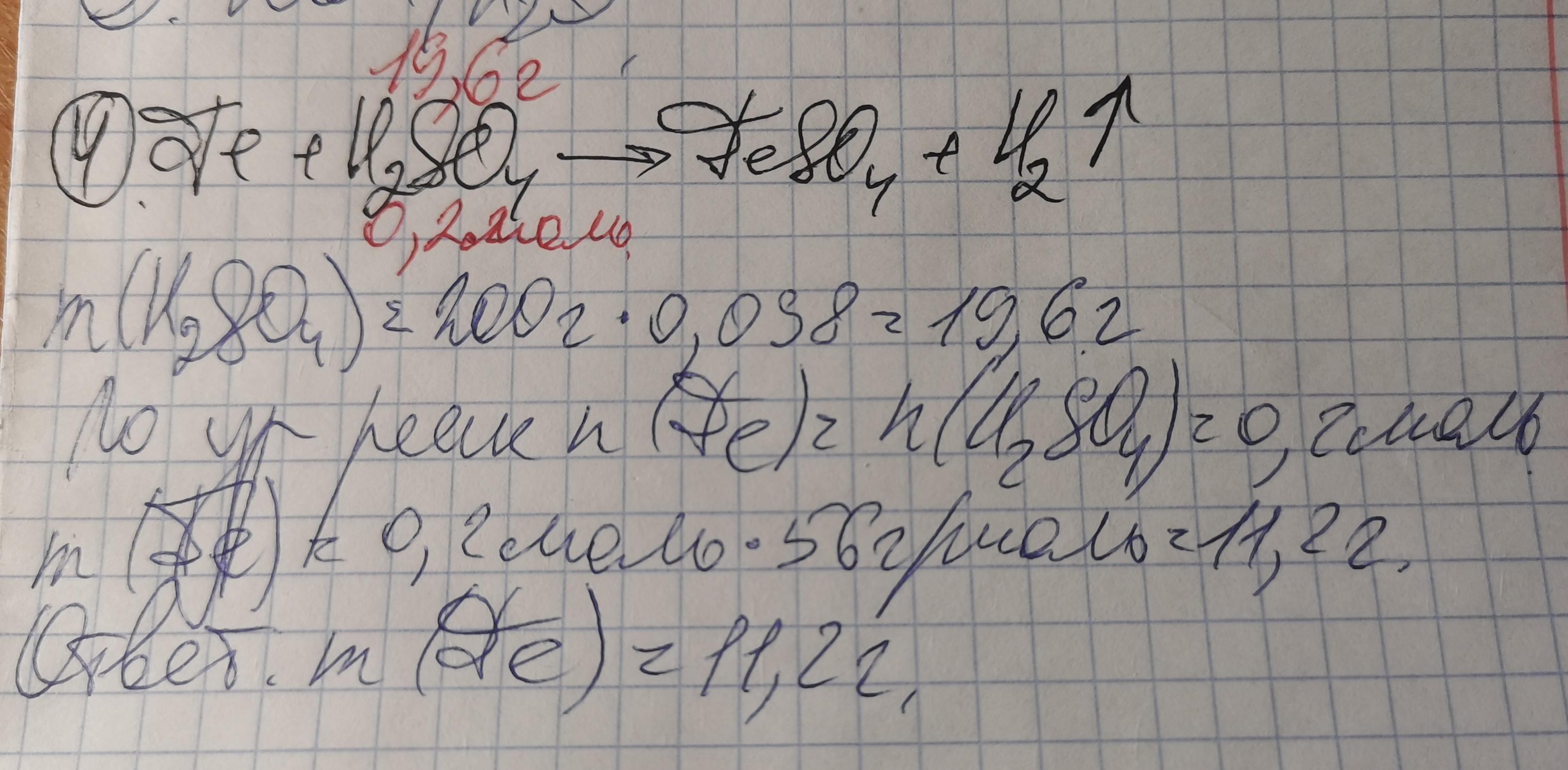
Похожие вопросы
Предмет: Русский язык,
автор: tixonovanata
Предмет: Английский язык,
автор: СофияЛапочка
Предмет: Русский язык,
автор: SashaSpilberg342
Предмет: Английский язык,
автор: dmitryankud777