Предмет: Химия,
автор: ElenaLomkina
При горении органического бескислородного вещества массой 23,54 г было получено 67,76 г углекислого газа, 17,82 мл воды и азот. Известно, что оно может вступить в реакцию с 3 моль брома в водном растворе. Определите молекулярную и структурную формулу вещества, составьте уравнение его реакции с избытком бромной воды.
Ответы
Автор ответа:
4
Ответ:
n(CO2)=67.76/44=1,54 моль n(H2O)=17.82/18=0,99 моль
m(C)=1.54*12=18,48 грамм m(H)=0.99*2=1,98 грамм m(N)=23.54-18.48-1.98=3,08
Доли компонентов в соединении
С - 18,48/(23,54*12)=0,06542
H - 1.98/23.54=0,0841
N - 3.08/(23.54*14)=0,00934
Отношение компонентов
С/H/N - 0,06542 /0,0841 /0,00934 - 7/9/1
С7H9N
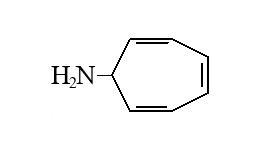
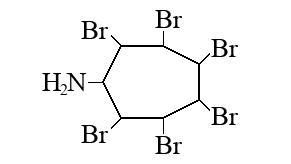
С 3 моль брома в водном растворе может вступить соединение с тремя двойными связями 1-амин циклгептатриен 2,4,6 (Циклогептатриен-2,4,6-иламин) в результат получится 2,3,4,5,6,7-гексабромциклогептанамин
C7H9N + 3Br2 = C7H9NBr6
Приложения:
Похожие вопросы
Предмет: Қазақ тiлi,
автор: Маралькуль
Предмет: Українська мова,
автор: borzenkova981
Предмет: Русский язык,
автор: kristinka971
Предмет: Алгебра,
автор: леле7