Предмет: Химия,
автор: verapustov
решить задачу(органика горение)
1. При сжигании образца органического вещества массой 3,48 г получено 7,04 г углекислого газа и 2,52 г воды. При нагревании с водным раствором гидроксида натрия данное вещество подвергается гидролизу с образованием двух продуктов – соли и этиленгликоля – в соотношении 2 : 1. На основании данных условия задания: 1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества и запишите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение реакции гидролиза исходного вещества в растворе гидроксида натрия
нашла соотношение 4:7:2 С4Н7О2-простейшая формула. не могу понять что за вещество.. как выглядит структурная формула
Ответы
Автор ответа:
2
Ответ:
1,2-O-дипропионилэтандиол-1,2
Объяснение:
Отношение элементов С/H/O - C4H7O2
Отношение вы правильно нашли, однако это вещество - сложный эфир этиленгликоля и у него должно быть 4 атома кислорода, домножаем на 2 и получаем 1,2-O-дипропионилэтандиол-1,2
Отношение элементов С/H/O - C8H14O4 - молярная масса 174 г/моль
По горению
2C8H14O4 + 19 O2 = 16 CO2 + 14 H2O
m(CO2)=(3.48/174)*8*44=7,04 грамма
m(H2O)=(3.48/174)*7*18=2.52 грамма
При щелочном гидролизе подобно гидролизу сложных эфиров глицерина получится сам этиленгликоль (1 моль) и пропионат натрия (2 моль)
C8H14O4+2NaOH=C2H6O2+2C3H5O2Na
Структурная формула
Приложения:
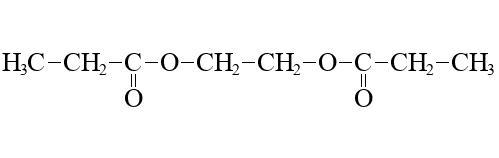
Похожие вопросы
Предмет: Русский язык,
автор: Vovaushakov
Предмет: Қазақ тiлi,
автор: Жорик07
Предмет: Другие предметы,
автор: т343
Предмет: Биология,
автор: galya620
Предмет: Алгебра,
автор: Hillg