Предмет: Химия,
автор: almazalmazov706
1. Из ниже перечисленных уравнения обратных реакций, выпишите те случаи, когда на основе изменения давления нарушается равновесие.
Попытайтесь обосновать ваше предложение.
Приложения:
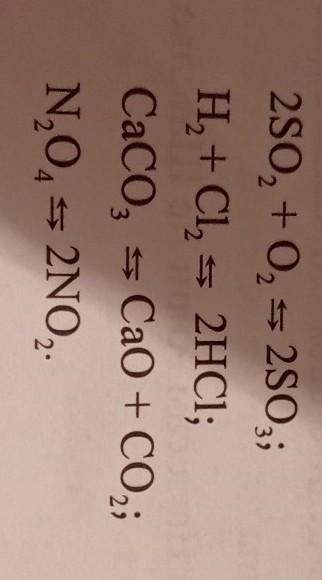
Ответы
Автор ответа:
1
Объяснение:
Принцип Ле Шателье - Брауна.
При увеличении давления химическое равновесия сместится в сторону прямой реакции, так как общее количество молекул уменьшается.
- 2SO2 + O2 = 2SO3, в реакцию вступила 3 молекулы газа, образовалась 2 молекулы. При увеличении давления равновесия сместится вправо, в сторону прямой реакции 2SO2 + O2 → 2SO3. При уменьшении давления равновесие сместится влево 2SO2 + O2 ← 2SO3.
- H2 + Cl2 = 2HCl Вступила в реакцию 2 молекулы, образовалось 2 молекулы. Увеличение или уменьшение давления не влияет на химическое равновесие.
- СаСО3 = СаО + СО2↑ При увеличении давления равновесия сместится влево СаСО3 ← СаО + СО2↑, при уменьшении вправо СаСО3 → СаО + СО2↑.
- N2O4 =2NO2 в реакцию вступила 1 молекулы газа, образовалась 2 молекулы. При увеличении давления равновесия сместится влево, в сторону обратной реакции N2O4 ← 2NO2. При уменьшении давления равновесие сместится вправо N2O4 → 2NO2
Похожие вопросы
Предмет: Қазақ тiлi,
автор: AlinaArt8
Предмет: Английский язык,
автор: DuyDuka
Предмет: Русский язык,
автор: fatya5
Предмет: Алгебра,
автор: HellOwl
Предмет: Математика,
автор: kiryushashaforostov