Предмет: Химия,
автор: М0Л0Т0В
ХИМИЯ ПЖ ХЭЛП!!!!!!!!!!!!!!!!!!!!
Приложения:
Ответы
Автор ответа:
2
Дано:
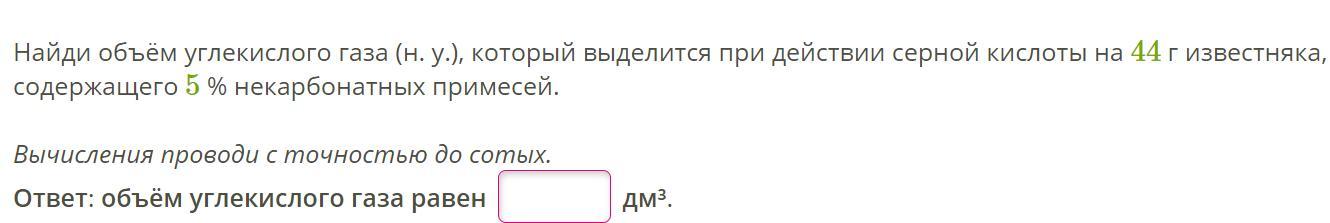
m(известняк CaCO3) = 44 г
ω(прим) = 5% = 0,05
Найти:
V(CO2)-?
Решение:
CaCO3+H2SO4⇒CaSO4+H2O+CO2
m(CaCO3) = 44 - 44 * 0,05 = 41,8 г
M(CaCO3) = 40 + 12 + 16*3 = 100 г/моль
n(CaCO3) = m/M = 41,8 /100 = 0,418 моль
n(CaCO3) = n (CO2) = 0,418 моль
Vm = 22.4 л/моль
V(CO2) = n*Vm = 0,418 * 22.4 = 9,36 дм³
Ответ: 9,36 дм³
М0Л0Т0В:
Не правильно!
Ведь написанно что в решениях надо до сотых всё
Я насчитал 55,10
(CaCO3) = 44- (44 * 10% /100%) =225 g
CaCO3+H2SO4-->CaSO4+H2O+CO2
M(CaCO3) =100 g/mol
n(CaCO3) = m/M = 245,6/100 =2,456
n(CaCO3) = n)CO2) = 2,46
V(CO2) = n*Vm =2,46 *22.4 = 55,104
CaCO3+H2SO4-->CaSO4+H2O+CO2
M(CaCO3) =100 g/mol
n(CaCO3) = m/M = 245,6/100 =2,456
n(CaCO3) = n)CO2) = 2,46
V(CO2) = n*Vm =2,46 *22.4 = 55,104
Вот
Верно, же?
Или я не прав?
Если не прав то сори за наезд
сравните ответ и решение, они отличаются
Похожие вопросы
Предмет: Русский язык,
автор: igor32rus
Предмет: Английский язык,
автор: belka83
Предмет: Русский язык,
автор: duborez1969
Предмет: Русский язык,
автор: Supermozgolom
Предмет: Химия,
автор: danilasd12