Предмет: Химия,
автор: Аноним
Быстрей пожалуйста дам 200 баллов
1. Определить количества вещества, массу, объем при (н.у) для
18,06 *1023 молекул углекислого газа (СO2).
2. Необходимо приготовить 500 г 25 % раствора соды. Какую массу воды и массу соды необходимо взять для приготовления раствора.
3. (*) Вычислите объем кислорода, который потребуется для сжигания порошка магния массой 12 г. (схема реакции: Mg + O2 ➝ MgO)
NikolayKhlestov:
Бро, ты на Online Gymnasium учишься?
Мы на одном курсе... Тоже проблемы с Химией?
Давай дружить. Ты дашь мне своё реальное имя и я тебе на сайте напишу!\
Давай дружить. Ты дашь мне своё реальное имя и я тебе на сайте напишу!\
Ответы
Автор ответа:
2
Объяснение:
1.n(CO2)=(18,06 *10^23)/6,02*10^23=3 моль
M(CO2) =12+16*2=44 г/моль
m(CO2) =44*3=132 г
V(CO2) =3*22,4 моль=67,2 л
2.mр.в =500*0,25=125 г - нужно взять соды
m(H2O) =500-125=375 г - нужно взять воды
Приложения:
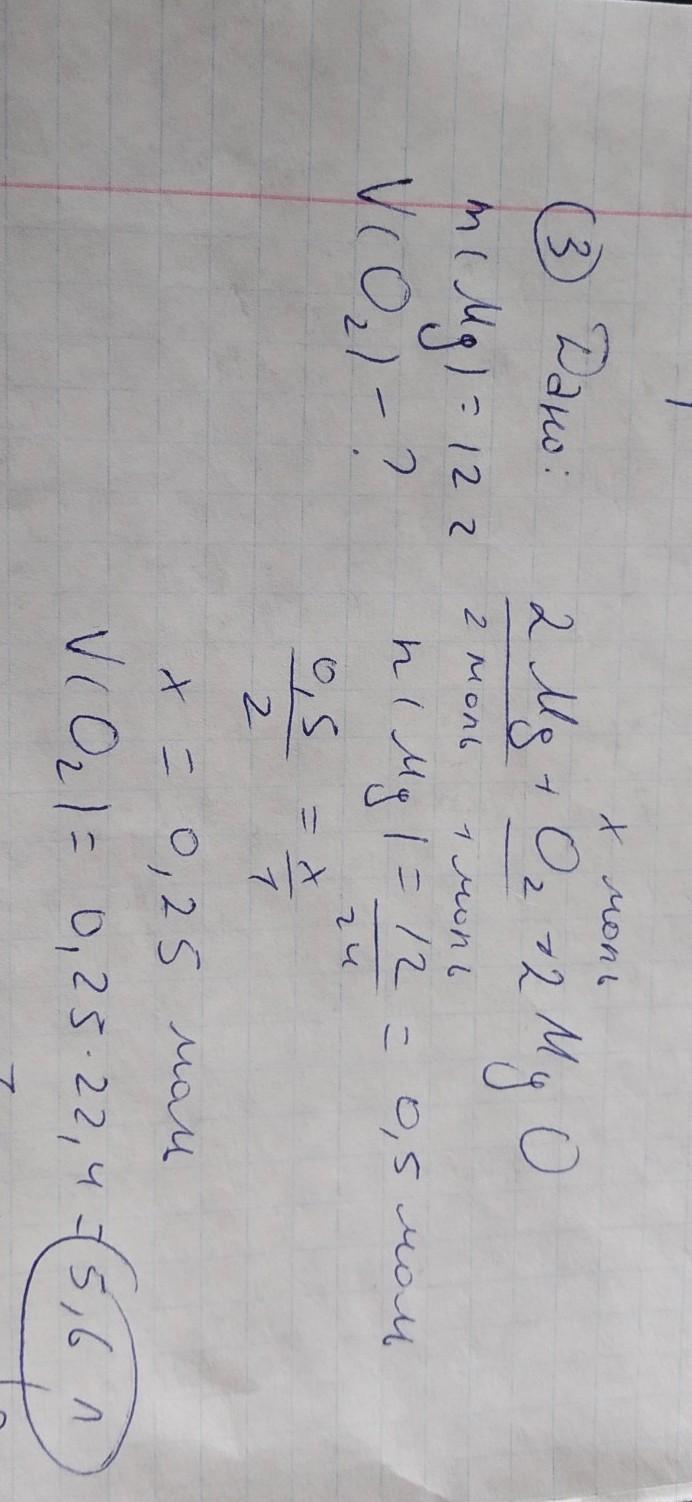
можете помочь с химией??
Определите массовые доли элементов соответствующих количественному составу дигидрофосфата натрия? Ответ приведите с точностью до целых.
Определите массовые доли элементов соответствующих количественному составу дигидрофосфата натрия? Ответ приведите с точностью до целых.
Похожие вопросы
Предмет: Английский язык,
автор: Ghostriley
Предмет: Русский язык,
автор: fnjfyn2001
Предмет: Окружающий мир,
автор: IgidaLove
Предмет: Алгебра,
автор: artem1275
Предмет: Қазақ тiлi,
автор: murashova285