Предмет: Химия,
автор: kamikazemeow
Рассчитайте объем (н.у) водорода, который выделится при взаимодействии магния с 98г раствора с массовой долей серной кислоты 10%
Ответы
Автор ответа:
0
Дано:
m(р-ра H2SO4)=98г
w(H2SO4)=10%
V(H2)-?
Решение:
1) Mg+H2SO4=MgSO4+H2
2) m(H2SO4)=98×0,1=9,8г
3) n(H2SO4)=9,8/(1×2+32+16×4)=0,1моль
4) по уравнению реакции n(H2SO4)=n(H2)=0,1моль
5) V(H2)=0,1×22,4=2,24л
Автор ответа:
0
Ответ:
2,24
..........................
Приложения:
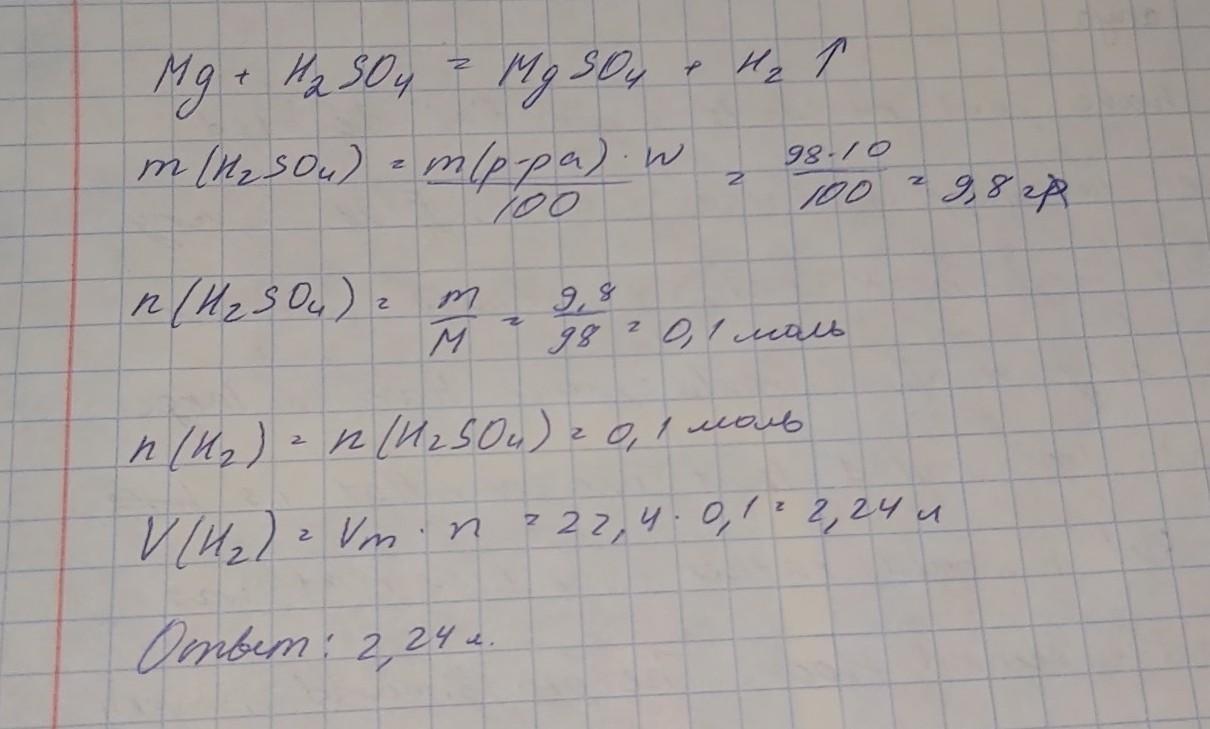
Похожие вопросы
Предмет: Русский язык,
автор: wolf12d
Предмет: Английский язык,
автор: АллаЧернова
Предмет: Английский язык,
автор: dimashchegolev2
Предмет: Русский язык,
автор: jugouna74
Предмет: Химия,
автор: anavyrodova767