Предмет: Химия,
автор: Shaherezada55
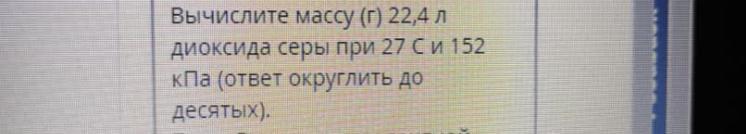
Помогите решить задачу , люди добрые :3
Приложения:
Ответы
Автор ответа:
1
Уравнение Менделеева-Клапейрона для идеального газа:
Р*V = m*R*T/M
где: Р - давление газа , Па. Р = 152 кПа = 152000 Па
V - объем газа, м³. V = 22,4 л = 0,0224 м³
m - масса газа, кг
R - универсальная газовая постоянная, R = 8,314 Дж/(моль*К)
T - температура, °К. T = 27 + 273 = 300°К
М - масса 1 моля газа, кг/моль. М(SO₂) = 32 + 2*16 = 64 г/моль =
0,064 кг/моль
Из уравнения находим массу:
m = Р*V*М/R *Т = 152000*0,0224*0,064/(8,314 *300) = 0,0874 кг = 87,4 г
Похожие вопросы
Предмет: Технология,
автор: violetta635vily
Предмет: Қазақ тiлi,
автор: nikasunko1nika
Предмет: Русский язык,
автор: Аноним
Предмет: Английский язык,
автор: Viking2001
Предмет: Русский язык,
автор: Jeforge