Предмет: Химия,
автор: hwanghyunjin2002skz
ПОМОГИТЕ ПОЖАЛУЙСТА СРОЧНО НУЖНО❗❗❗❗
Рассчитайте объем водорода,выделившегося при взаимодействии 30г цинка с 200 мл 20%-ного раствора соляной кислоты
Приложения:
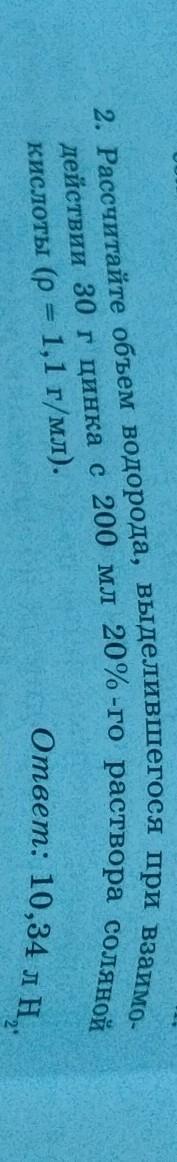
Ответы
Автор ответа:
1
Ответ:
10.34л водорода
Объяснение:
m(Zn)= 30г
V(HCl)=200мл
p(HCl)=1.1г/мл
w(HCl)=20%
V(H2)=?
m(HCl)=V•p=200•1.1=220г
m(HCl)=mp-pa•w(HCl)=220•0.2= 44г
n(HCl)=m:M=44:36.5=1.2моль
n(Zn)=m:M=30:65=0.46моль
n(HCl)=1/2n(H2)=0.6 моль
n(Zn)=n(H2)=0.46 моль
- соляная в избытке, расчеты продолжаем по недостатку, по цинку.
Zn + 2HCl = ZnCl2 + H2↑
n(HCl)=1/2n(H2)=0.6 моль
n(Zn)=n(H2)=0.46 моль
V(H2)=n(H2)•Vm=0.46•22.4=10.34л
Похожие вопросы
Предмет: Математика,
автор: lizav2000
Предмет: Математика,
автор: Буше6
Предмет: Русский язык,
автор: hsyrca
Предмет: Химия,
автор: Diru07