Решите пожалуйста до вечера


Ответы
Ответ:
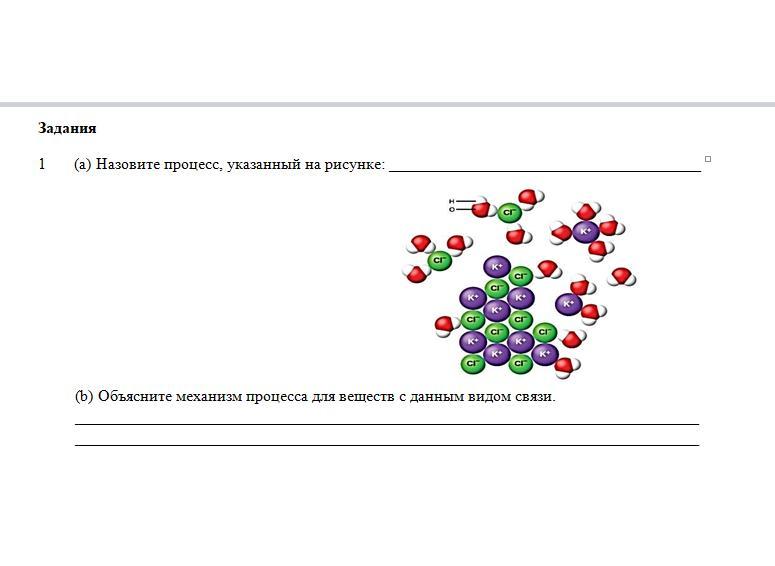
1) а) электролитическая диссоциация;
b) механизм процесса заключается в том, что при растворении вещества в воде происходит его распад на ионы.
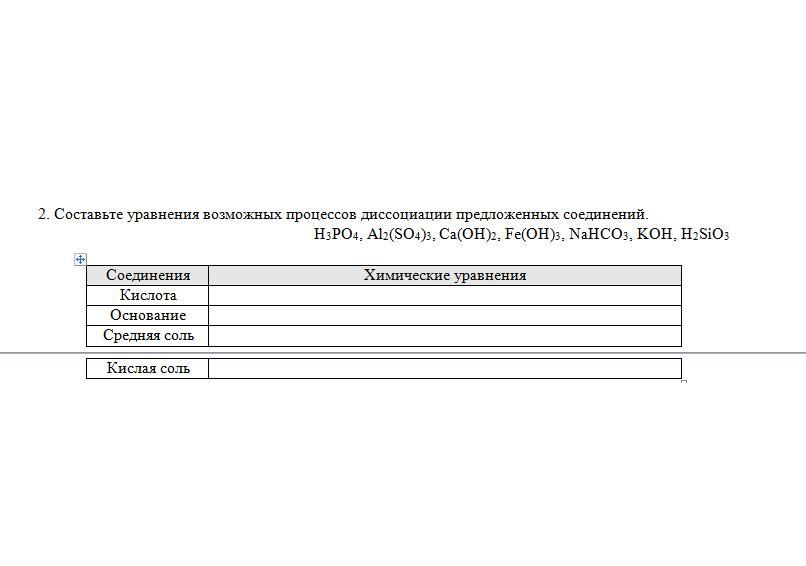
2) кислоты: H3PO4 - слабая кислота и слабый электролит, поэтому не диссоциируется в воде;
H2SiO3 - слабая и к тому же нерастворимая в воде, слабый электролит, также диссоциация не происходит;
основания: Zn(OH)2, Fe(OH)3 - не растворимы в воде => слабые электролиты, не диссоциируются
KOH = K(+) + OH(-)
кислая соль: KHCO3 = K(+) + HCO3(-)
средняя соль : Al2(SO4)3 = 2Al(3+) + 3SO4(2-)
3) 1) соляная кислота и гидроксид натрия - выделится вода
2) хлорид железа и гидроксид натрия - выпадет осадок
4)
а) K2SiO3 + 2HCl → 2KCl + H2SiO3
б)Al(OH)3 + 3HCl → AlCl3 + 3H2O
в)HCl+NaOH=H2O+NaCl (можешь взять любой вариант реакции нейтрализации)
г)CaCO3+2HCl= CaCl2+CO2+H2O
5)
Я предполагаю что это сульфид алюминия
Al2S3+H2O= Al(OH)2+ + H+ HS- OH-
Катион Алюминий 3+
Анион Сера 2-
Формула Al2S3
Доказательство
Al2S3 + H2O <> 2Al3+ + 3S2-
Al + H2O <> AlOH + H
S + H <> HS
AlOH + H2O <> Al(OH)2 + H
HS + H > H2S
Al(OH)2 + H2O > Al(OH)3 + H
Среда нейтральная, после реакции кислая