Предмет: Химия,
автор: nastz11
Если можно , то через дано и решение !!!Рассчитайте массу сульфата натрия, которое образуется при нейтрализации раствора содержащего 80 г гидроксида натрия растворной кислоты
Ответы
Автор ответа:
0
Решение:
m(NaOH)=80g
Mr(NaOH)=23+16+1=40
M(NaOH)=40g/mol
n(NaOH)=80g/40g/mol=2 mol
2 mol x
2NaOH+H2SO4=Na2SO4+2H2O
2 1
2/2=x/1
x=1
n(Na2SO4)=1 mol
Mr(Na2SO4)=142
M(Na2SO4)=142g/mol
m=n*M
m(Na2SO4)=1*142=142g
Ответ 142 г
m(NaOH)=80g
Mr(NaOH)=23+16+1=40
M(NaOH)=40g/mol
n(NaOH)=80g/40g/mol=2 mol
2 mol x
2NaOH+H2SO4=Na2SO4+2H2O
2 1
2/2=x/1
x=1
n(Na2SO4)=1 mol
Mr(Na2SO4)=142
M(Na2SO4)=142g/mol
m=n*M
m(Na2SO4)=1*142=142g
Ответ 142 г
Автор ответа:
0
Решение задачи на фото.
Приложения:
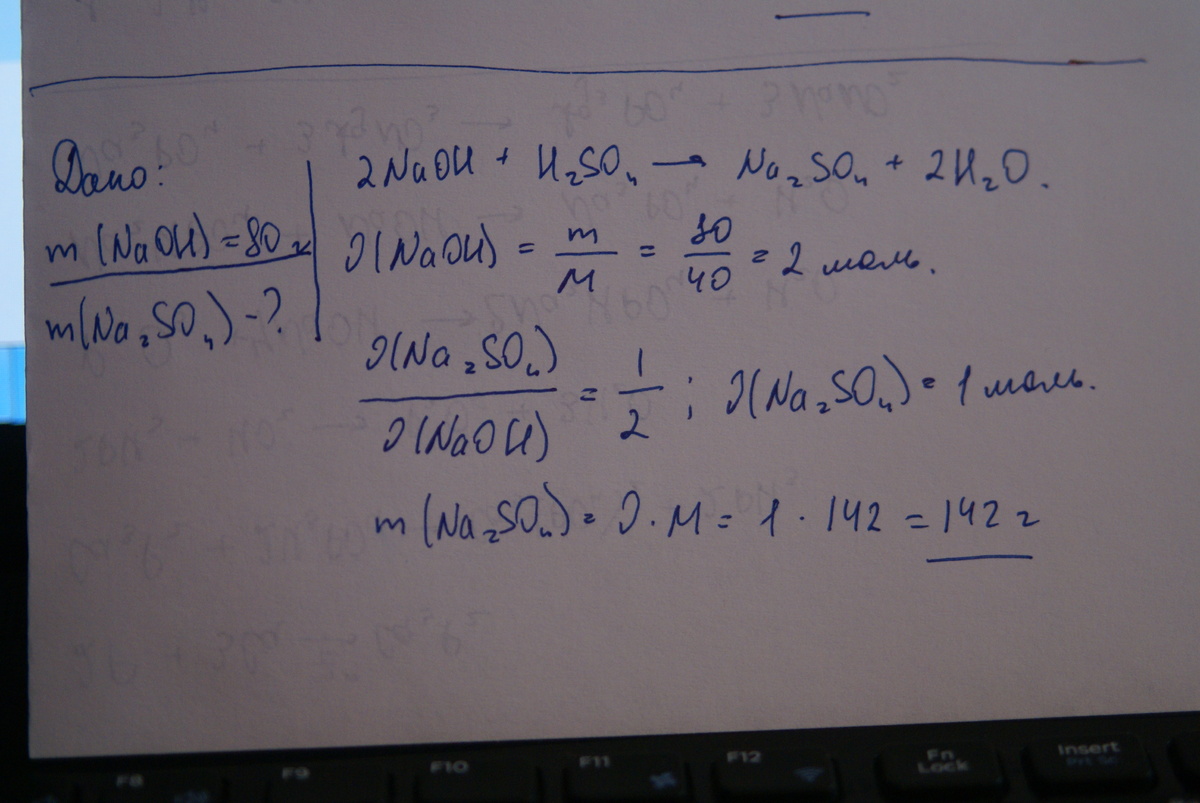
Похожие вопросы
Предмет: География,
автор: aleshandart
Предмет: Қазақ тiлi,
автор: rekaterina84
Предмет: Физкультура и спорт,
автор: jsisjs73
Предмет: Математика,
автор: МеГаМоЗг01
Предмет: Геометрия,
автор: valeriaAleksis