Предмет: Химия,
автор: kytcyme
Помогите пожалуйста очень надо
Приложения:

Ответы
Автор ответа:
0
Объяснение:
No 3 - см. рис.
4. Ответ: 0,88 г СО2
см. на рис.
5. Дано: *
Решение. Согласно закону сохранения масс,
То же верно и относительно массы НCl в растворе:
Масса НCl вычисляется по ф-ле
Отсюда:
Обозначим массу 1-го р-ра как х, 2-го как у. Тогда:
Получаем систему:
То есть изначально взяли:
x = 150 г 30% р-ра НCl
y = 450 г 10% р-ра НCl
Ответ:
150 г 30% р-ра НCl
450 г 10% р-ра НCl
*индекс fin обозначает параметры финального раствора - взят исключительно чтобы не спутать с начальными параметрами
Приложения:

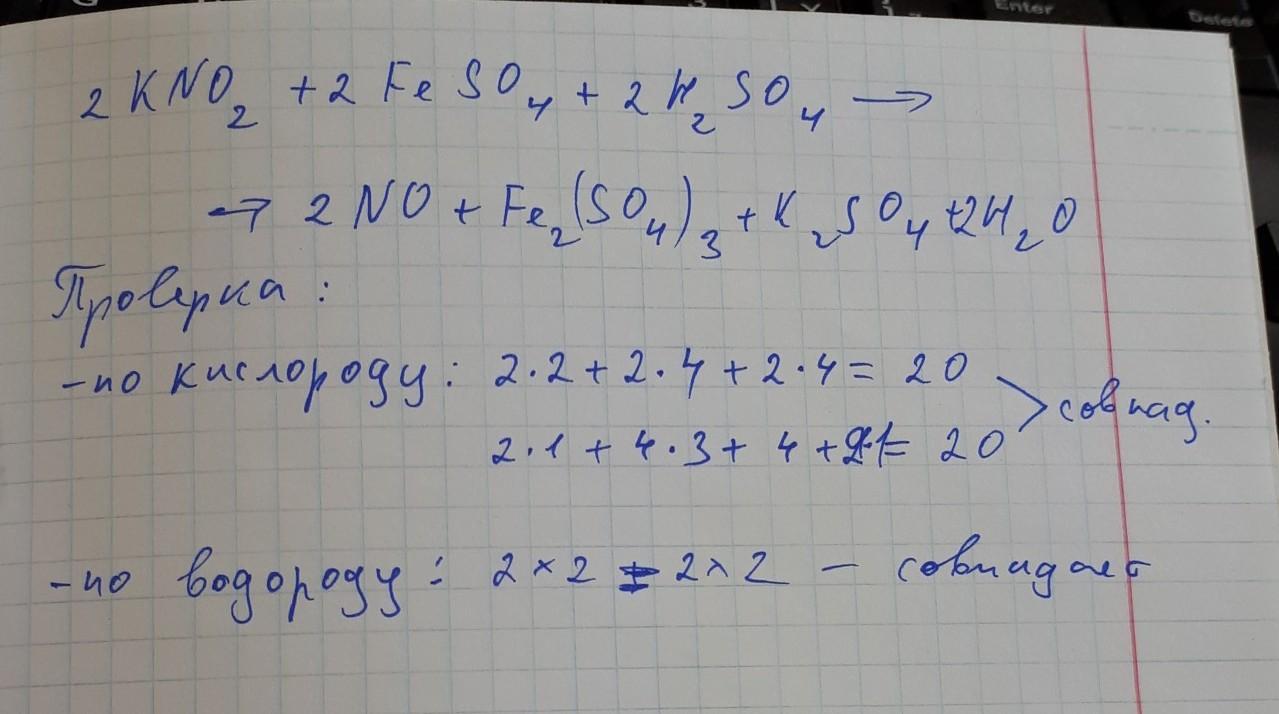

Похожие вопросы
Предмет: Английский язык,
автор: Марет85
Предмет: Русский язык,
автор: Аноним
Предмет: Русский язык,
автор: паа2
Предмет: Биология,
автор: илья1968