найти массу железа которая образуется при взаимодействии 32 г оксида железа (|||) и 8,96 л угарного газа
Ответы
Ответ: 14,9 г
Решение во вложении
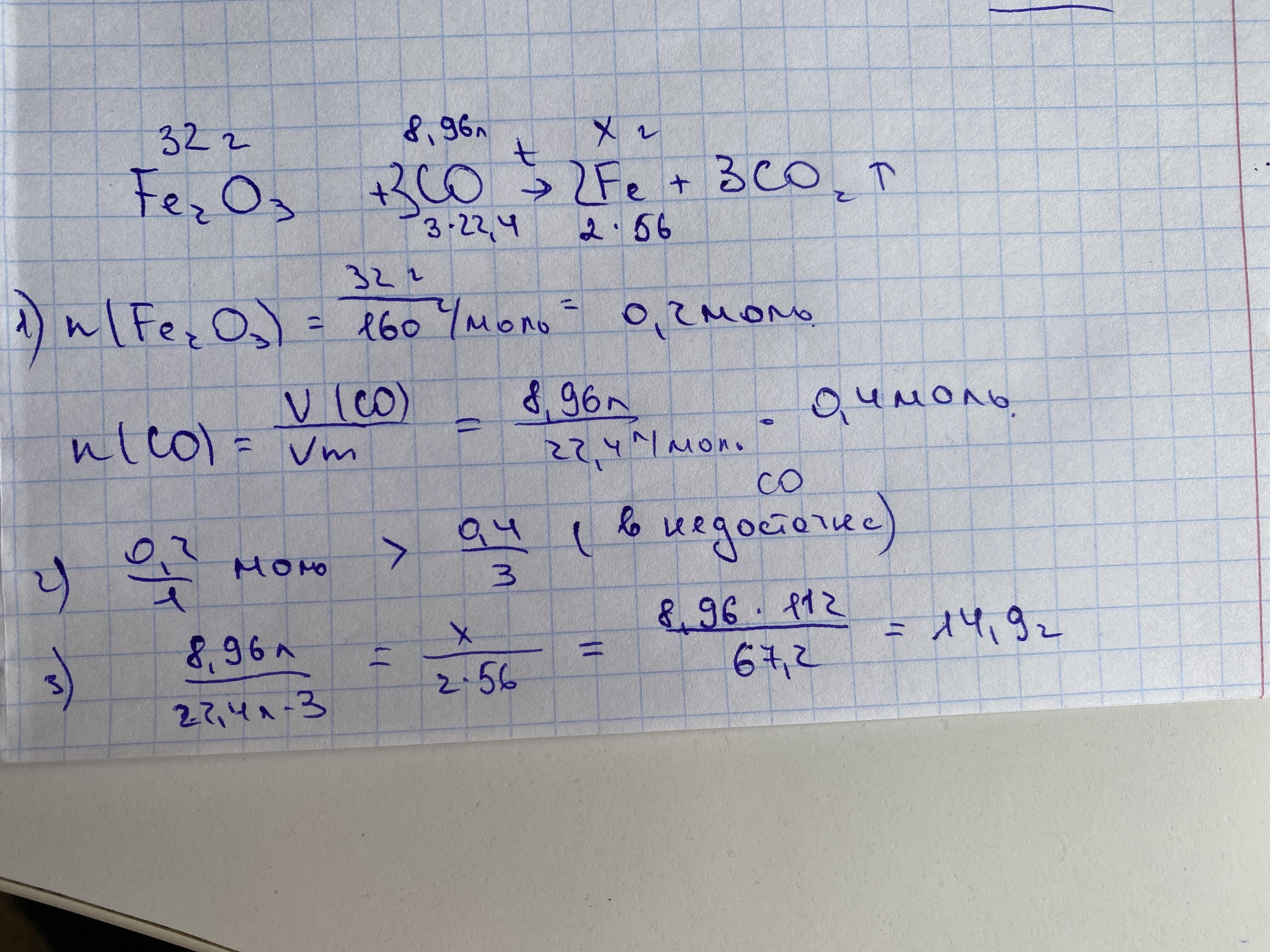
Дано:
m (Fe2O3) = 32г
V (CO) = 8,96л
Vm = 22,4 л/моль
Найти:
m (Fe) - ?
Решение:
Fe2O3 + 3 CO → 2 Fe + 3 CO2 (реакция ОВР)
1) Найдём молярную массу оксида железа (3):
M (Fe2O3) = 56*2 + 16*3 = 160 г/моль
2) Найдём количества вещества Fe2O3 по формуле:
n (Fe2O3) = m/M = 32/160 = 0,2 моль
3) Найдём молярную массу Fe по периодической таблице Менделеева:
M (Fe) = 56 г/моль
4) n (Fe2O3) относится к n (Fe), как 1:2, значит:
n (Fe) = 0,2*2 = 0,4 моль
5) Находим массу железа по формуле:
m (Fe) = n * M = 0,4 * 56 = 22,4г
6) Находим n (CO):
n (CO) = V/Vm = 8,96/22,4 = 0,4 моль
7) n (CO) относится к n (Fe), как 1,5:1, значит:
n (Fe) = 0,4:1,5=0,27
8) Находим массу железа (настоящую, раньше был недостаток):
m (Fe) = 56 * 0,27 = 14,9г
Ответ: 14,9г