Предмет: Химия,
автор: danilmoskalchenko35
2. Рассчитайте объем 30%-й (р = 1,156 г/мл) соляной кис-
лоты, необходимой для получения 6,72 лхлора, при ее
взаимодействии с диоксидом марганца.
помогите пожалуйста с этим заданием . пожалуйста не что попало
Ответы
Автор ответа:
4
Ответ:
Смотри ниже.
Объяснение:
Приложения:
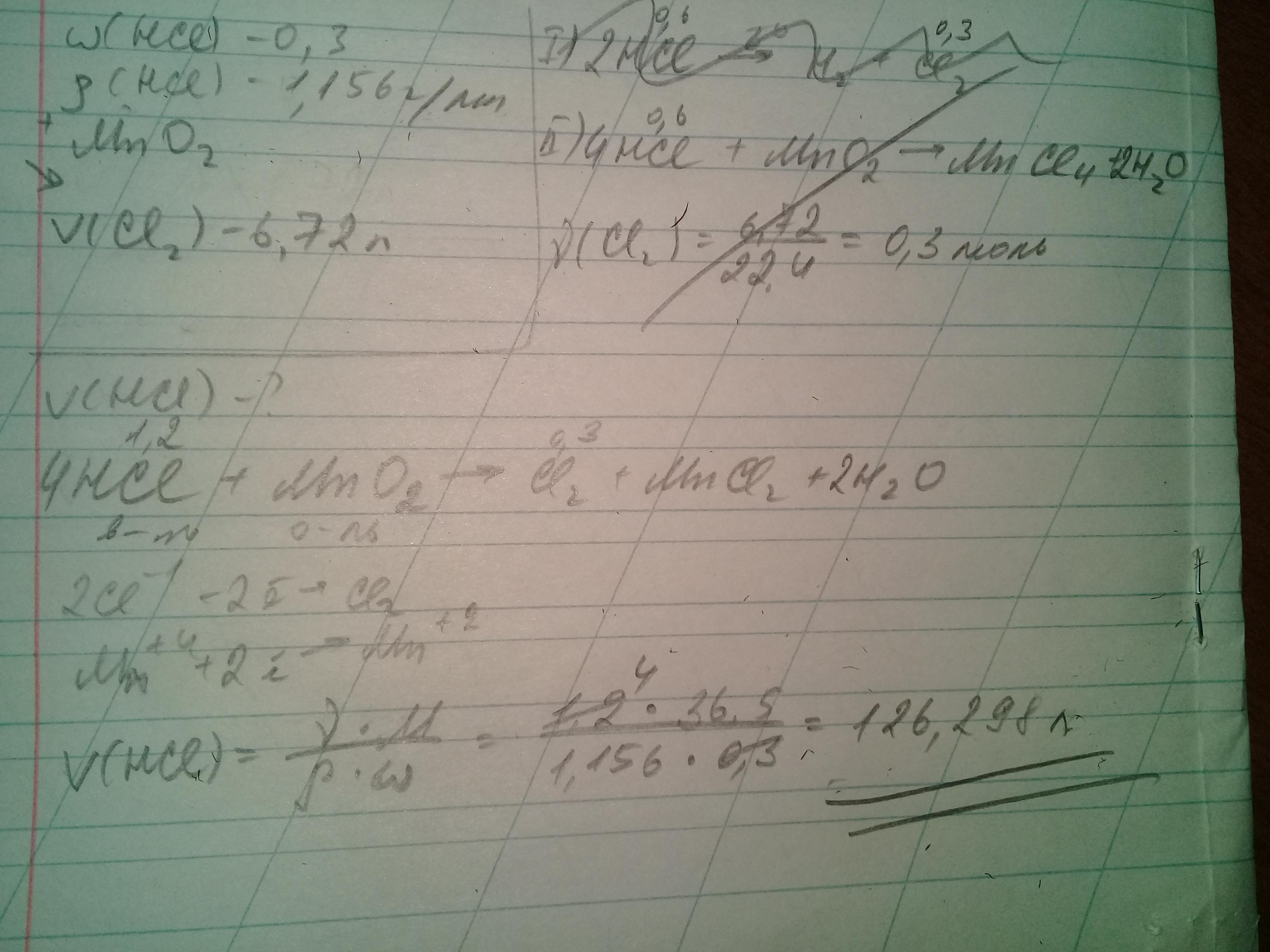
спасибо большое
Автор ответа:
3
Ответ:
Объяснение:
4HCl+MnO2=Cl2+MnCl2+2H2O
n(Cl2)=V/Vm=67,2/22,4=3моль
n(HCl)=4n(Cl2)=4*3=12моль
m(HCl)=12*36,5=438г
mр-ра(HCl)=438/0,3=1460г
Похожие вопросы
Предмет: Русский язык,
автор: серый1985
Предмет: Окружающий мир,
автор: ZaZkol
Предмет: Русский язык,
автор: sony27
Предмет: Математика,
автор: Winne
Предмет: Русский язык,
автор: dinbili77
n(Cl2)=V/Vm=67,2/22,4=3моль
n(HCl)=4n(Cl2)=4*3=12моль
m(HCl)=12*36,5=438г
mр-ра(HCl)=438/0,3=1460г