Помогите Пожалуйста.
Ответы
Ответ:
Объяснение:
10)
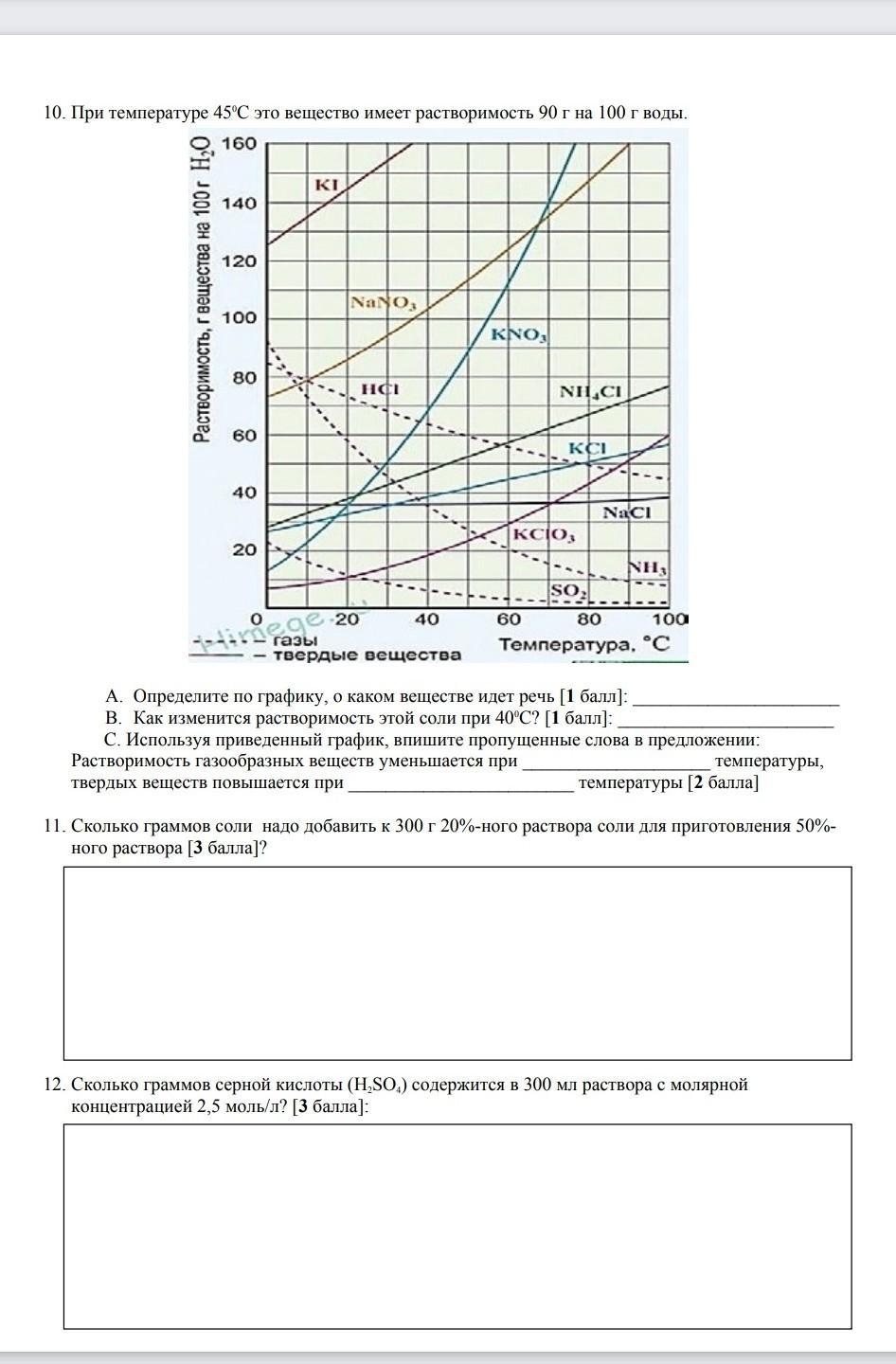
А) KNO3 - нитрат калия , но в условии ошибка. При такой температуре он имеет растворимость 80 г / 100 г ( по графику). Ближайших веществ в этой точке на графике нет, поэтому подходит только KNO3 .
В) Растворимость понизится. При 40° растворимость составит 70 г / 100 г H2O вместо 80 г /100г при 45° .
С) Растворимость газообразных веществ уменьшается при повышении температуры, твердых веществ повышается при увеличении температуры.
11) Дано:
m(раствора соли) = 300 г
w1(соли) = 20% = 0.2
w2(соли) = 50% = 0.5
Найти: m(соли доб.) - ?
Решение:
Масса соли, которую нужно добавить к 20%-ному раствору, чтобы получить раствор 50% = х г
m(соли в растворе 20%) = m(раствора соли) * w1(соли) = 300 г * 0.2 = 60г
Масса соли в новом растворе: (60 + х) г ;
Масса нового раствора : (300 + х) г ;
Массовая доля соли в новом растворе : 0.5
0.5 = (60 + х) / (300 + х) | * (300 + х)
(300 + х) * 0.5 = (300 + х) * (60 + х) / (300 + х)
150 + 0.5x = 60 + x
- 0.5 x = - 90 | * ( - 1 )
0.5 x = 90
x = 90 / 0.5
x = 180 (г)
Ответ: 180 г
12) Дано:
V(раствора H2SO4) = 300 мл = 0.3 л
См(H2SO4) = 2.5 моль / л
Найти: m(H2SO4) - ?
Решение:
Cм(H2SO4) = m(H2SO4) : M(H2SO4) : V(раствора H2SO4)
m(H2SO4) = Cм(H2SO4) * M(H2SO4) * V(раствора H2SO4)
m(H2SO4) = 2.5 моль / л * 98 г/моль * 0.3 л = 73.5 г
Ответ: 73.5 г