Предмет: Химия,
автор: liabrahamyan
Сколько литров углекислого газа необходимо для получения 250 г CaCO₃ ?
Ответы
Автор ответа:
1
Ответ: 56 л
Объяснение:
Приложения:
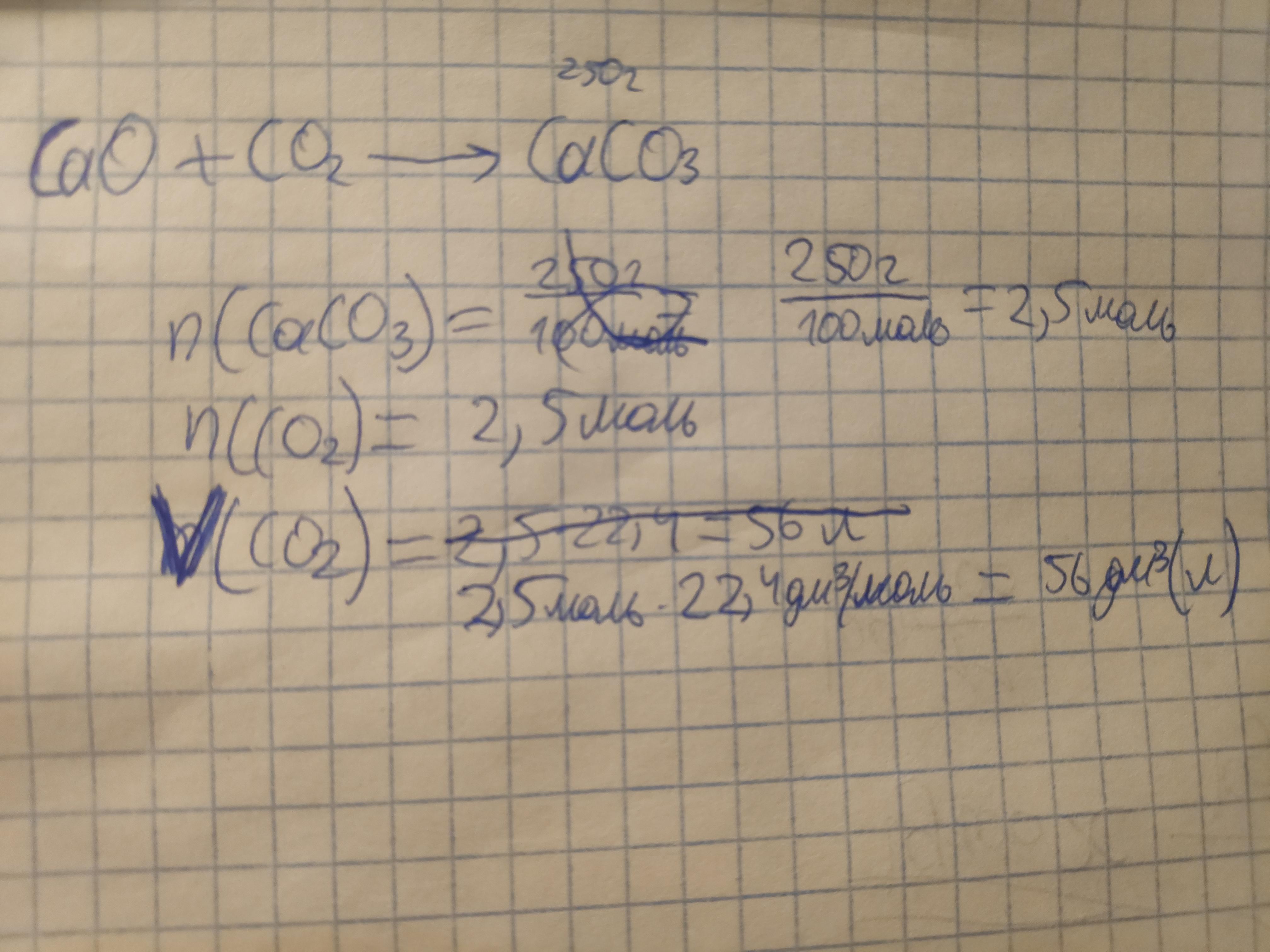
Автор ответа:
1
Ответ: Х л 250г
CaO+ CO2= CaCO3
1 моль 1 моль
22,4л/ моль 100г/моль
Vm( CO2)= 22,4 л/моль
M(CaCO3) =40+12+16*3=100г/моль
n= m/M n(CaCO3)= 250г: 100г/моль=2,5моль
n(CO2)=n(CaCO3)=2,5моль - по ур-ю
V(CO2)= Vm *n V(CO2) 22,4л/моль*2,5моль= 56л
Ответ: 56л
Объяснение:
Похожие вопросы
Предмет: Математика,
автор: dbva
Предмет: Алгебра,
автор: Кариночка78
Предмет: Математика,
автор: bandorenkol
Предмет: Алгебра,
автор: valandil
Предмет: Информатика,
автор: NameXD