Предмет: Химия,
автор: vasilking197
Помогите пожалуйста с задачами:
В реакцию с хлоридом свенца вступил цинк массой 6,5 грам. Сколько грам хлорида цинка образовалось при этом.
Вычислите объём углекислого газа который образовался при взаимодействии 24 грам углерода с кислородом.
Буду очень благодарна.
Ответы
Автор ответа:
0
,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,
Приложения:
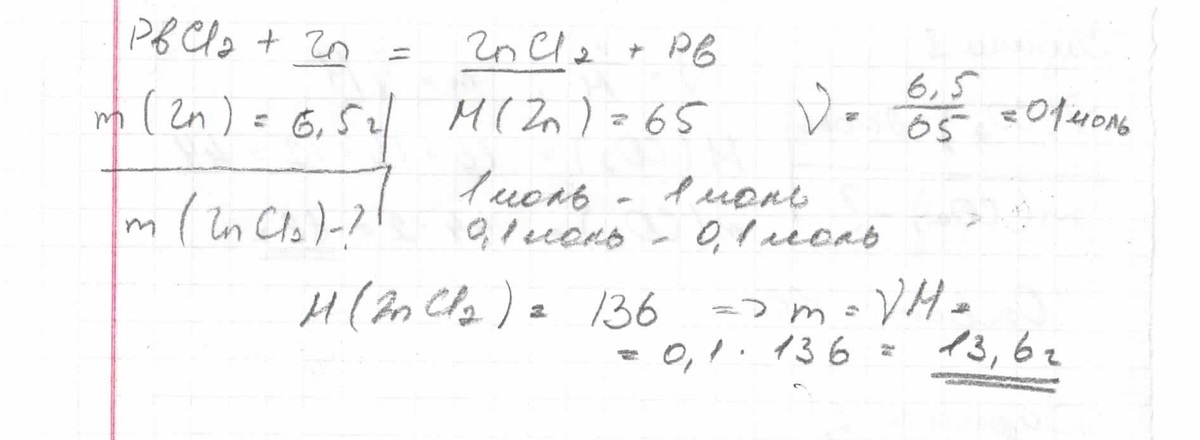
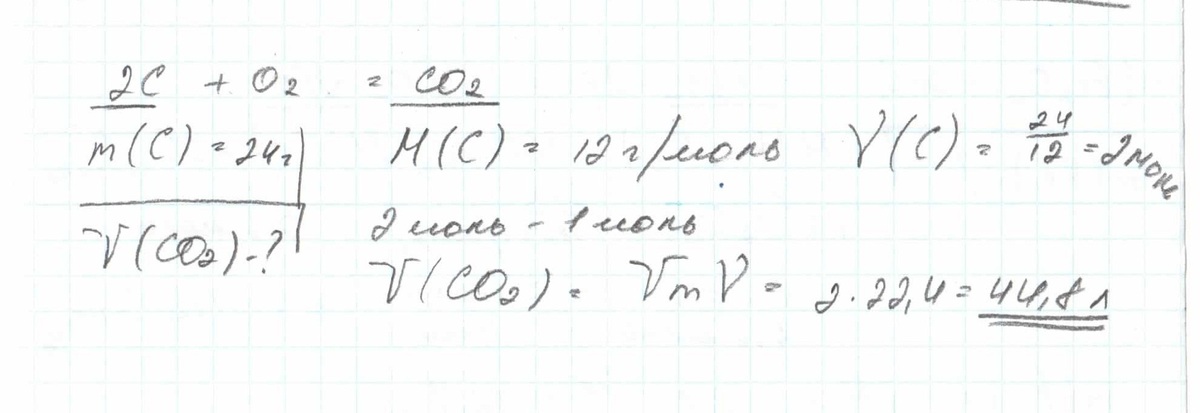
Автор ответа:
0
1)
PbCl2+Zn=ZnCl2+Pb
M(Zn)=65г/моль
n(Zn)=6.5/65=0.1моль
n(Zn)=n(ZnCl2)=0.1моль
M(ZnCl2)=135г/моль
m(ZnCl2)=n*M=135*0.1=13.5г
Образовалось 13.5г хлорид цинка
2)
C+O2=CO2
n(C)=24/12=2моль
n(C)=n(CO2)=2моль
V(CO2)=2*22.4=44.8л
Образовалось 44.8л углекислого газа
PbCl2+Zn=ZnCl2+Pb
M(Zn)=65г/моль
n(Zn)=6.5/65=0.1моль
n(Zn)=n(ZnCl2)=0.1моль
M(ZnCl2)=135г/моль
m(ZnCl2)=n*M=135*0.1=13.5г
Образовалось 13.5г хлорид цинка
2)
C+O2=CO2
n(C)=24/12=2моль
n(C)=n(CO2)=2моль
V(CO2)=2*22.4=44.8л
Образовалось 44.8л углекислого газа
Приложения:
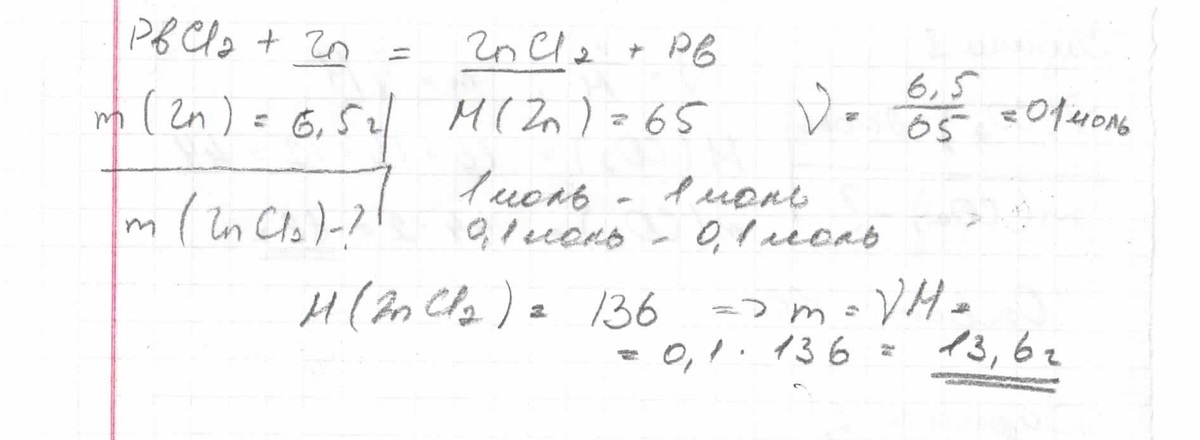
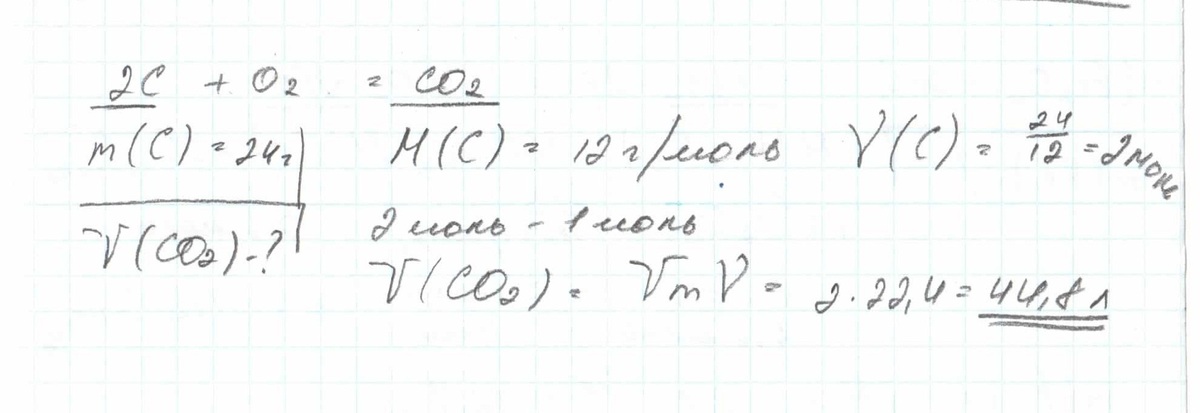
Похожие вопросы
Предмет: Математика,
автор: Richi0770
Предмет: Математика,
автор: 5508180es
Предмет: Математика,
автор: katastroganova2006
Предмет: Алгебра,
автор: Helptome