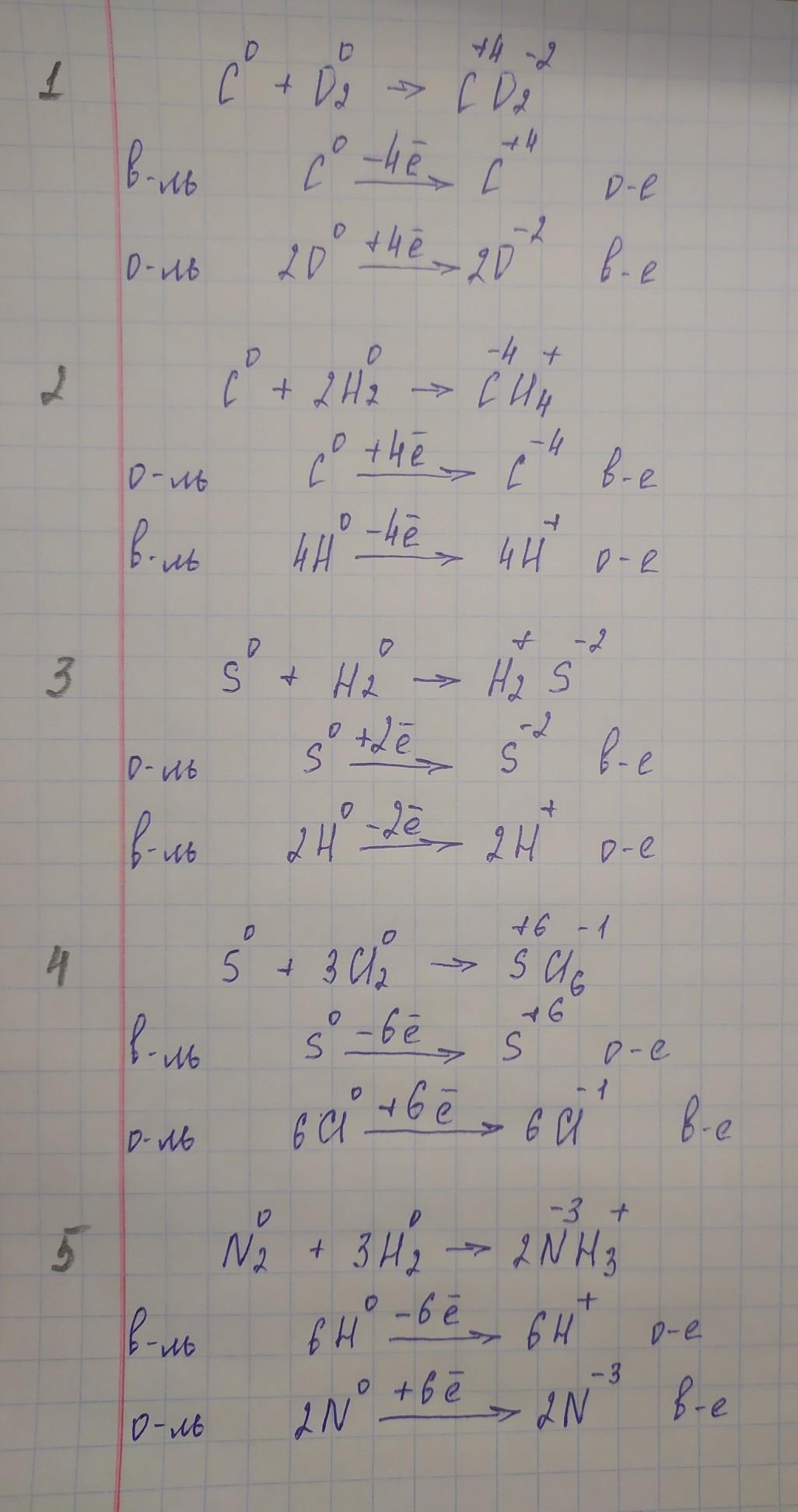1. Расставить степени окисления элементов, определяют окислитель восстановитель:
C + O2 = CO2
C + 2H2 = CH4
S + H2 = H2S
S + 3Cl2 = SCl6
N2 + 3H2 = 2NH3
Ответы
Ответ:
C - восстановитель + O2 - окислитель = C(+4)O2(2-)
C - окислитель + 2H2 - восстановитель = C(-4)H4 (+)
S - окислитель + H2 - восстановитель = H2(+)S(-2)
S - восстановитель + 3Cl2 - окислитель = S(+6)Cl6 (-)
N2 - окислитель + 3H2 - восстановитель = 2N(-3)H3(+)
Объяснение:
У простых веществ степень окисления 0, подпишите наверху, я решил не указывать, ибо понятно, что степень окисления равна 0
Я запоминал так, если перед нами окислитель, значит процесс восстановление, если перед нами восстановитель, значит процесс окисление
Восстановитель - повышает степень окисления (отдаёт электроны)
Окислитель - понижает степень окисления (принимает электроны)
Процесс окисления - увеличение степени окисления
Процесс восстановления - уменьшение степени окисления
Объяснение:
В-ль = восстановитель
В-е = восстановление
О-ль = окислитель
О-е = окисление