Предмет: Химия,
автор: hovepac276
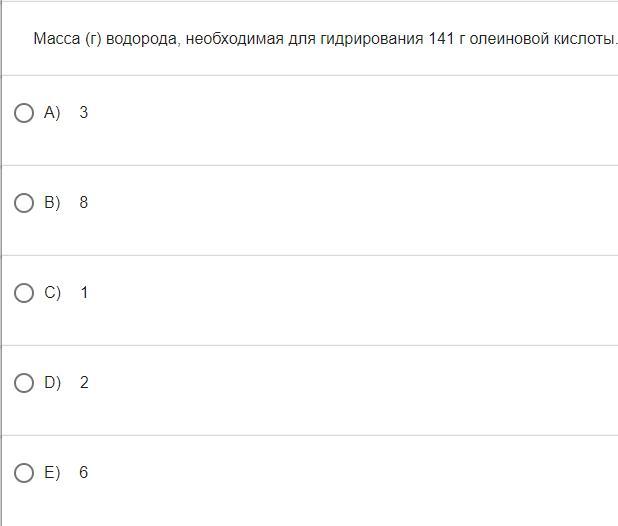
Масса (г) водорода, необходимая для
гидрирования 141 г олеиновой кислоты.
Приложения:
Ответы
Автор ответа:
1
Дано:
m(C₁₇H₃₃COOH) = 141г
Найти: m(H₂) - ?
Решение:
Для начала составим уравнение реакции:
ᅠᅠ
Найдём количество вещества олеиновой кислоты:
ᅠᅠ моль
По уравнению реакции перейдём к количеству вещества водорода:
ᅠᅠ моль
Найдём массу водорода:
ᅠᅠ грамм
Ответ: С) 1.
Похожие вопросы
Предмет: История,
автор: Аноним
Предмет: Алгебра,
автор: buyanovanastya
Предмет: Английский язык,
автор: DEiMAKENZ
Предмет: Геометрия,
автор: Ocлиk
Предмет: Физика,
автор: Catqshakate2003