Предмет: Химия,
автор: ArianaG
Помогите пожалуйста кто сможет.
Определить массу BaSO4 которая образуется при взаимодействии H2SO4 массой 9,8г с BaCl2 массой 16,8 г.
Ответы
Автор ответа:
0
Уравнение реакции: BaCl2 + H2SO4 = BaSO4↓ + 2HCl
Находим количества реагентов:
v(H2SO4) = 9,8 г : 98 г/моль = 0,1 моль.
v(BaCl2) = 16,8 г : 208 г/моль = 0,08 моль.
Серная кислота в избытке, считаем по BaCl2.
По уравнению реакции, количество BaSO4 равно v(BaCl2).
Находим массу BaSO4:
m(BaSO4) = 0,08 моль * 233 г/моль = 18,64 г.
Находим количества реагентов:
v(H2SO4) = 9,8 г : 98 г/моль = 0,1 моль.
v(BaCl2) = 16,8 г : 208 г/моль = 0,08 моль.
Серная кислота в избытке, считаем по BaCl2.
По уравнению реакции, количество BaSO4 равно v(BaCl2).
Находим массу BaSO4:
m(BaSO4) = 0,08 моль * 233 г/моль = 18,64 г.
Автор ответа:
0
Спасибо, спасли :)
Автор ответа:
0
Не за что)
Автор ответа:
0
получает вообще 18,64
но я думаю стоит округлить до 19!
:)
но я думаю стоит округлить до 19!
:)
Приложения:
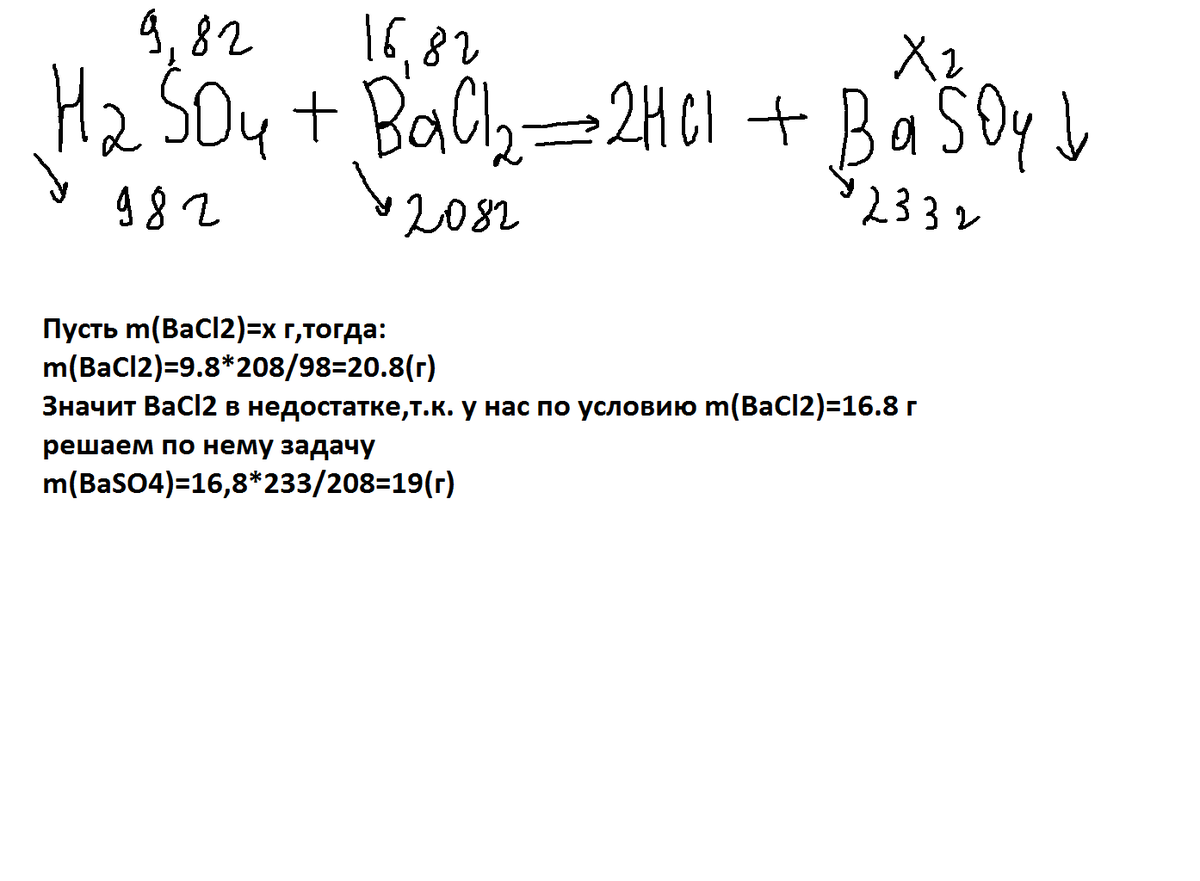
Автор ответа:
0
И Вам спасибо :)
Автор ответа:
0
обращайся;)
Похожие вопросы
Предмет: Русский язык,
автор: Аноним
Предмет: Русский язык,
автор: Аноним
Предмет: Математика,
автор: Аноним
Предмет: Геометрия,
автор: mouse007