Предмет: Химия,
автор: supergames368
При сгорании 4,95 г органического вещества в качестве единственных продуктов сгорания образовались углекислый газ массой 14,3 г и вода массой 2,25 г.
Известно,что при гидролизе данного соединения в щелочной среде образуются две соли.
1 проведите необходимые вычисления и установите молекулярную формулу исходного органического вещества
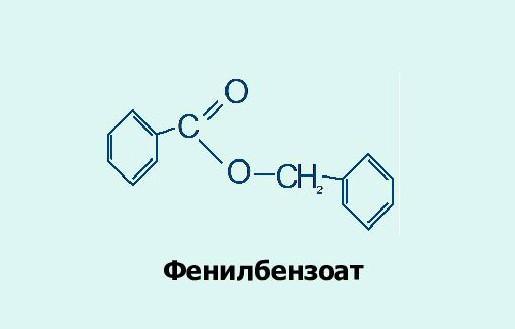
2 составьте структурную формулу этого вещества ,которая однозначно отражает порядок связи атомов в его молекуле
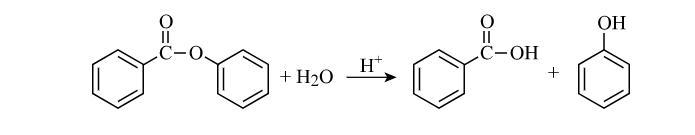
3 напишите уравнение гидролиза вещества в присутствии соляной кислоты.
Ответы
Автор ответа:
2
Ответ:
n(CO2) = m/M= 14,3/44= 0,325 моль
Откуда n(C)= n(CO2)= 0.325 моль
m(C) = 12г/моль * 0,325 моль = 3,9 г
n(H2O) = m/M = 2,25г/18 г/моль = 0.125 моль
n(H)= 2n(H2O) = 0.125 моль * 2 = 0,25 моль
m(H) = 0.25моль * 1г/моль 0,25 г
В данном соединение присутствует кислород, поэтому m (O) = m (в-ва) - m(C) - m(H) =0,8 г
Количество вещества кислорода
n(O)= 0.8г/16 г/моль = 0,05 моль
n(C):n(H):n(O) = 0.325: 0,25 : 0,05 = 6,5: 5 : 1 = 13: 10: 2
С13 H10 O2 -истинная формула данного соединения
Исходным веществом является фенилбензоат
И реакция гидролиза фенилбензоата:
Объяснение:
Приложения:
supergames368:
Спасибо вам большое!!!
Похожие вопросы
Предмет: Английский язык,
автор: Boombeen
Предмет: Английский язык,
автор: artemii100
Предмет: Русский язык,
автор: dimonn29
Предмет: География,
автор: вопросник134
Предмет: Алгебра,
автор: Alelexus