Предмет: Химия,
автор: Waggon
Из 16г оксида железа (3) аюмотермией получили 10 г железа. Какова массовая доля выхода железа от теоретически возможного?
Ответы
Автор ответа:
0
Лови решение друг))джчьимпдво
Приложения:
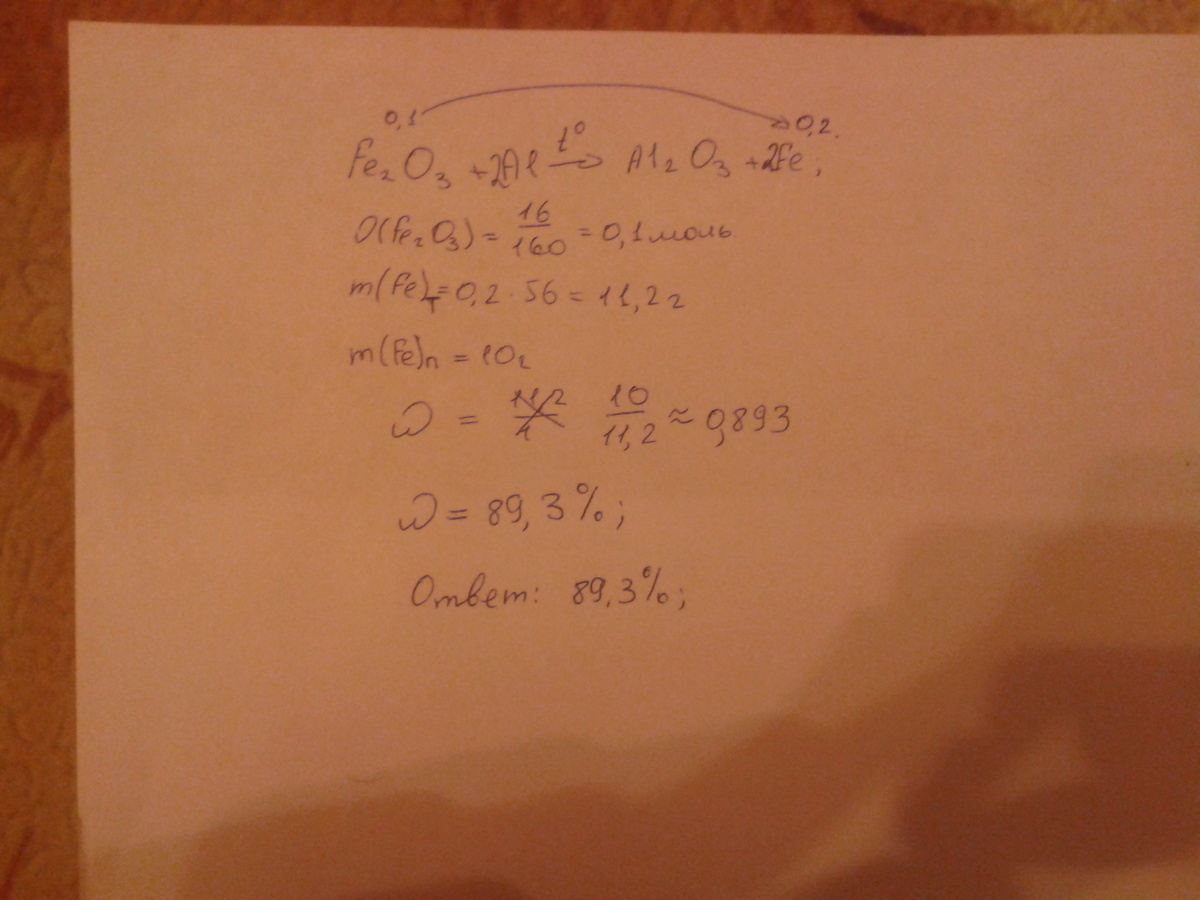
Автор ответа:
0
немного не то ты сделал. Зачем ушел в массу.
Автор ответа:
0
Fe2O3 + 2Al = Al2O3 + 2Fe
n( практическая) = 1056 = 0,17 моль.
Ищем теоретическую:
n( Fe2O3) = 16160 = 0,1 моль
По уравнению реакции пересчитываем на моли чистого железа, видно, что его в два раза больше, значит n ( теоретическая) = 0,1*2 = 0,2 моль.
w выхода = m практическая m теоретическая = 0,17 0,2 = 0,85 = 85%
n( практическая) = 1056 = 0,17 моль.
Ищем теоретическую:
n( Fe2O3) = 16160 = 0,1 моль
По уравнению реакции пересчитываем на моли чистого железа, видно, что его в два раза больше, значит n ( теоретическая) = 0,1*2 = 0,2 моль.
w выхода = m практическая m теоретическая = 0,17 0,2 = 0,85 = 85%
Приложения:
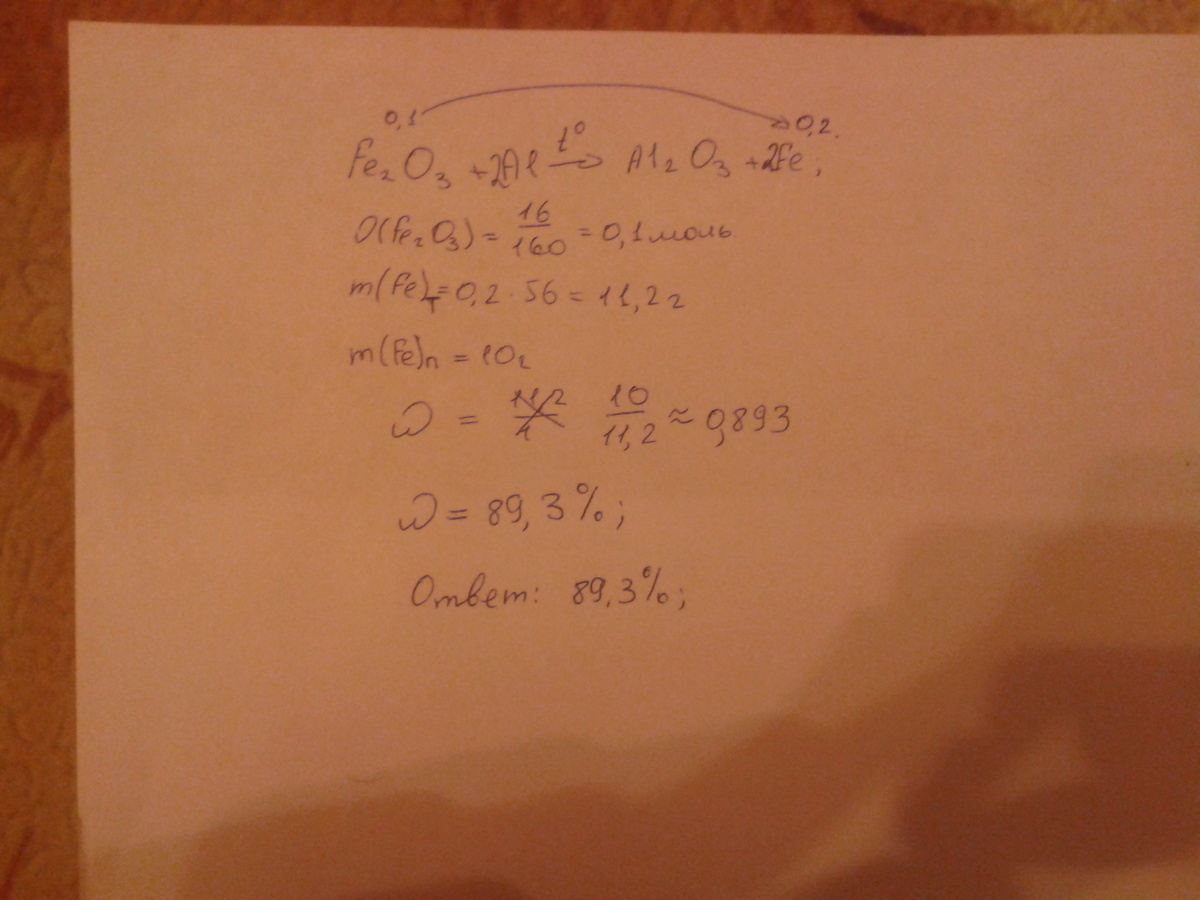
Похожие вопросы
Предмет: Математика,
автор: Аноним
Предмет: Английский язык,
автор: niki56857
Предмет: Информатика,
автор: filoh86277
Предмет: Информатика,
автор: lllulllu
Предмет: Математика,
автор: max123225