Решите пожалуйста.
Химия 8 класс
Ответы
Ответ:
Задание 1
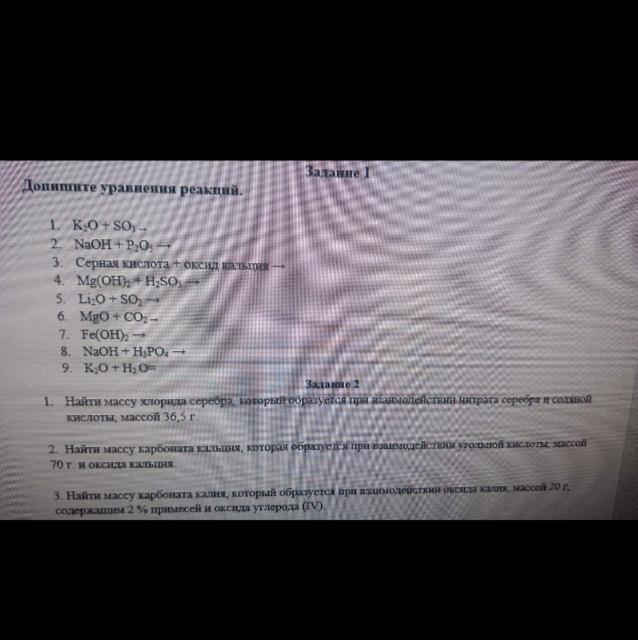
K20+S03= K2SO4
3NaOH+P2O5=2Na3P04
H2S04 (серная кислота) + CaO (оксид кальция) = CaS04 + H20
Mg(OH)2+ H2SO3 = MGS03 + 2H20
Li2O+SO2 = Li2S03
MgO+CO2= MgCO3
Fe(OH)2 = FeO+ H20
3NaOH+H3P04 = Na3PO4 +3H20
K2O+ H20 = 2KOH
Объяснение:
1. В первом случае взаимодействуют основный оксид с кислотным оксидом (основной - это оксиды металлов со степенью окисления +1, +2, кислотные - это оксиды неметалла или оксиды металла со степенью окисления больше +4)
2. Щелочь (Щелочь - растворимое в воде основание) взаимодействует с кислотным оксидом+ мы уравняли все это.
3. Кислота взаимодействует с основным оксидом, реакция обмена.
4. Гидроксид взаимодействует с кислотой.
5. Взаимодействие основного с кислотным оксидом.
6. Основный оксид взаимодействует с кислотным оксидом.
7. Нерастворимые основания разлагаются при нагревании на оксид металла + воду.
8. Щелочь взаимодействует с кислотой.
9. При взаимодействие основного оксида с водой образуется основание.
Со вторым заданием не смогу помочь, извини =(
Ответ:
Объяснение:
1) K2O + SO3 = K2SO4
6NaOH + P2O5 = 2Na3PO4 + 3H2O
H2SO4 + CaO = CaSO4 + H2O
Mg(OH)2 + H2SO4 = MgSO4 + 2H2O
Li2O + SO2 = Li2SO3
MgO + CO2 = MgCO3
Fe(OH)2 -> FeO + H2O
3NaOH + H3PO4 = Na3PO4 + 3H2O
K2O + H2O = 2KOH
36,5 г Х г
2) AgNO3 + HCl = AgCl + HNO3
n=1 моль n=1 моль
М=36,5 г/моль М = 143,5 г/моль
m=36,5 г m=143,5 г
36,5 г HCl - Х г AgCl
36,5 г HCl - 143,5 г AgCl
m(AgCl) = 36,5 * 143,5 / 36,5 = 143,5 г
70 г Х г
3) CaO + H2CO3 = CaCO3 + H2O
n=1 моль n=1 моль
М = 62 г/моль М = 100 г/моль
m=62 г m=100 г
70 г Н2СО3 - Х г СаСО3
62 г Н2СО3 - 100 г СаСО3
m(CaCO3) = 70 * 100 / 62 =113 г