помогите срочно, хотябы 2 задачи!!!!!!
дам все что хотите
спасибо + лучший ответ

Ответы
Объяснение:
1. NO2: у N +4, у О -2. Fe(OH)3: У Fe +3 (можно быстро вычислять значение с.о. у металла в основании, зная, что с.о. гидроксильной группы ОН -1, т.е. в данном случае Fe = 3 * 1, а так как металл и он отдаёт электроны, то с.о. положительная) у О -2, у Н +1. Н2SiO3: у Н +1, у О -2, у Si +4. BaSO4: у Ba +2, у O -2, у S +6.
2. Cl2O7 – оксид, так как бинарное соединение элемента менее электроотрицательное, чем кислород с кислородом О в его степени окисления -2. FeCl3 – соль так как соединение кислотного остатка Сl (от НCl образовался) с металлом Fe. Н2S – кислота, так как состоит из кислотного остатка S и водорода. СО2 – аналогично по объяснению Cl2O7 оксид. Fe(OH)3 – основание так как соединение гидроксильной группы ОН с металлом. Н2SiO3 – кислота так как соединение кислотного остатка (тут SiO3) с водородом. КNO3 – соль так как соединение кислотного остатка (тут NO3, образовавшийся от кислоты NNO3) с металлом К. Са(ОН)2 – основание, т.к. ОН – гидроксильная группа, а Са – металл.
3. Cl2O5 (цифра после формулы значит валентность хим. элемента с переменной с.о.) LiOH (как мы запомнили с.о. у ОН -1, а значит валентность 1, у Лития так как он в 1А группе постоянно валентность 1) Сu(NO3)2 – нитрат по сути название кислотного остатка, из-за валентности меди = 2 и валентности NO3 (это полезно запомнить), равной 1, нужно два кислотного остатка на одну медь в молекуле, оттого (NO3)2. (Na)3PO4 – аналогично составляем соль: фосфат – кислотный остаток PO4 с валентностью 3, его же и в формулировке названия первым записывают (фосфат ...), а также Na, имеющий постоянную валентность 1 из-за положения в таблице. Т.о. для равности валетностей (пары электронные общие ж создают) три Na. Серная кислота – Н2SO4, так как у Н валетность 1, у SO4 2. Оксид углерода 4 – СО2, так как у оксида по опр. О 2 валентность, а по названию у С 4. Гидроксид кальция – СаОН, т.к. у Са постоянная валетность 2 (находится в 2А группе и является щелочноземельным металлом) Сульфат (т.е. соль серной кислоты Н2SO4) кальция – СаSO4. Азотистая кислота – НNO2. Карбонат (соль угольной кислоты Н2CO3 с валетностью кислотного остатка 2) кальция – СаСО3.
4. Дано:
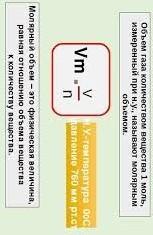
нормальные условия (н.у.) => p = 760 мм.рт.ст. и t = 0°С => молярный объём газа V0 = (смотри внизу) м^3/моль
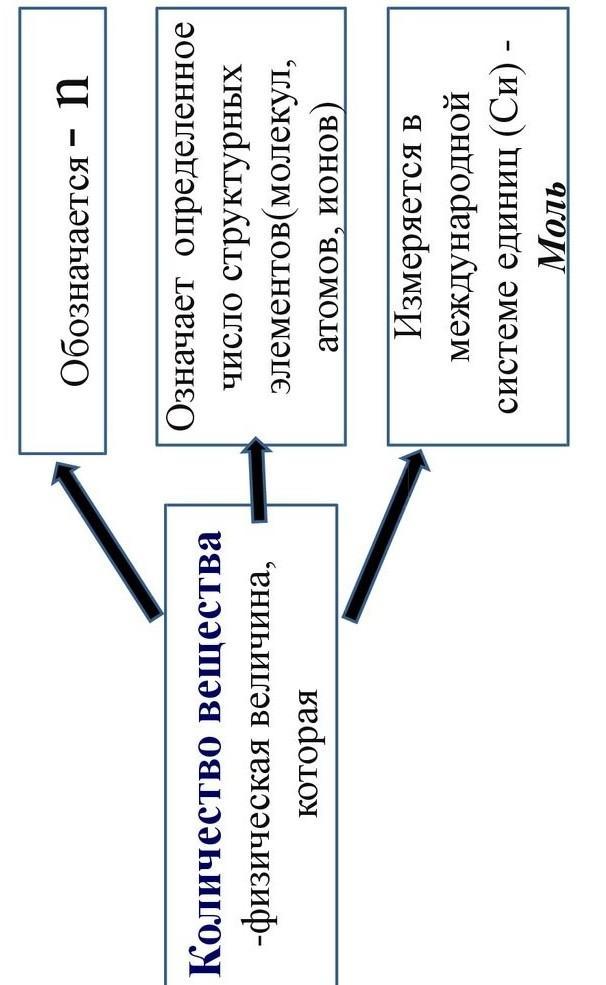
Молярный объём газа – физ-ая величина, показывающая объём, который занимает любой газ количеством вещества 1 моль. При н.у. его величина нам известна. Оксид азота 2 – NO, его масса нам известна, по формуле можно посчитать его молярную массу(М) численно равную относительной молекулярной массе т.е. сумме произведений относительной атомной массы (ОАМ) хим-ого элемента на кол-во его атомов в молекуле. У нас всё так: M(NO) = ОАМ(N) * 1 (в молекуле 1 атом азота содержится) + ОАМ(О) * 1(аналогично 1 атом кислорода в 1 молекуле) = 14*1 + 16*1 = 30 г/моль. Теперь можно высчитать количество вещества(газа) n. n = m/М (масса на молекулярную массу). У нас: n = 20/30 = 2/3 моль. Объём V газа можно высчитать так: V = V0 * n =
= 0.01493 ~~ (значок "примерно равно", округление) 0.015 м^3 (метр в кубе)
По поводу четвёртой задачи прилагаю справочный материал сверху, если что, на последней картинке количество вещества просто v обозначили, обычно это n, но бывают разные обозначения, воттт.