Заполните таблицу АХОВ
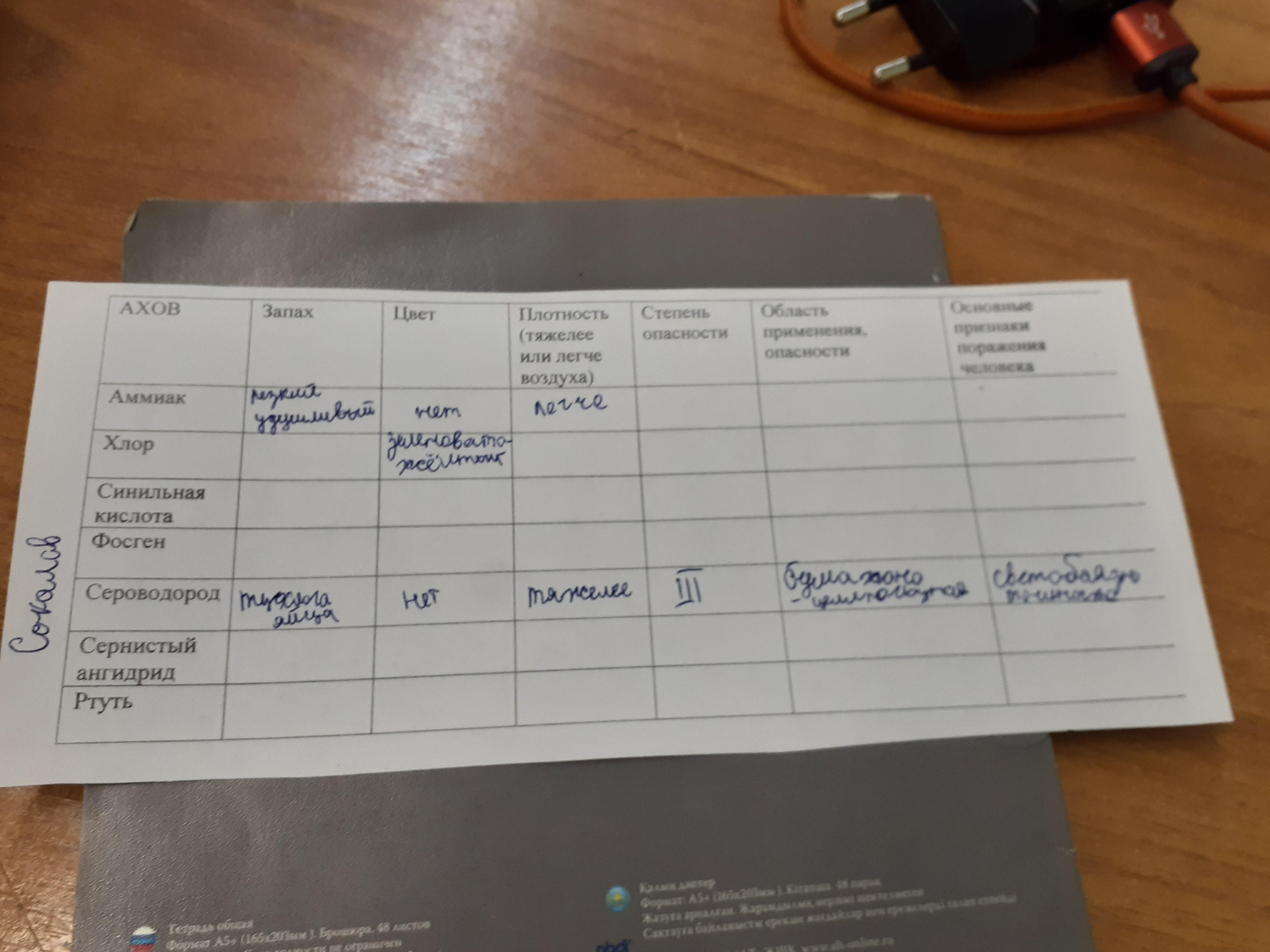
Ответы
Ответ:
Объяснение:
1 2 3 4 5 6
1. Аммиак NH₃ резкий, нет, легче, токсичен в медицине
производство
минеральных
удобрений
2. Хлор CI₂ хлор при нормальных условиях — ядовитый газ желтовато-зелёного цвета, тяжелее воздуха, с резким запахом и сладковатым, «металлическим» вкусом. Хлор — токсичный удушающий газ, при попадании в лёгкие вызывает ожог лёгочной ткани, удушье. У животных и человека ионы хлора участвуют в поддержании осмотического равновесия, хлорид-ион имеет оптимальный радиус для проникновения через мембрану клеток. Хлор применяют во многих отраслях промышленности, науки и бытовых нужд: Оконный профиль, изготовленный из хлорсодержащих полимеров .
Основным компонентом отбеливателей является. В производстве поливинилхлорида, пластикатов, синтетического каучука, из которых изготавливают: изоляцию для проводов, оконный профиль, упаковочные материалы, одежду и обувь, линолеум и грампластинки, лаки, аппаратуру и пенопласты, игрушки, детали приборов, строительные материалы.Отбеливающие свойства хлора известны с давних времен. Хлор идет для производства хлорорганических инсектицидов — веществ, убивающих вредных для посевов насекомых, но безопасных для растений. Использовался как боевое отравляющее вещество, а также для производства других боевых отравляющих веществ: иприт, фосген.
3. Синильная кислота HCN
4. Фосген COCl₂
5. Сероводород H₂S
6. Сернистый газ SO₂
7. Ртуть Hg
Примечание: надо выбрать отсюда для заполнения таблицы.
1. Опасность аммиака Аммиак токсичен. По физиологическому действию на организм относится к группе веществ удушающего и нейротропного действия, способных при ингаляционном поражении вызвать токсический отёк лёгких и тяжёлое поражение нервной системы. Пары аммиака сильно раздражают слизистые оболочки глаз и органов дыхания, а также кожные покровы. Это человек и воспринимает как резкий запах. Пары аммиака вызывают обильное слезотечение, боль в глазах, химический ожог конъюнктивы и роговицы, потерю зрения, приступы кашля, покраснение и зуд кожи.
3. Синильная кислота HCN бесцветная, очень летучая, легкоподвижная ядовитая жидкость, имеющая характерный запах горького миндаля. Синильная кислота содержится в некоторых растениях, коксовом газе, табачном дыме, выделяется при термическом разложении нейлона, полиуретанов.
Синильная кислота является веществом, вызывающим кислородное голодание тканевого типа. В результате тканевой гипоксии, развивающейся под влиянием синильной кислоты, в первую очередь нарушаются функции центральной нервной системы. Действие: результате острого отравления наблюдается резкое увеличение частоты и глубины дыхания, развивается одышка, проникая в кровь, синильная кислота снижает способность клеток воспринимать кислород из притекающей крови.
4. Фосген COCl₂ Фосген представляет собой бесцветный газ, чрезвычайно токсичный и удушливый газ с запахом прелого сена. 3,9 РАЗА ТЯЖЕЛЕЕ ВОЗДУХА. Обладает удушающим действием. Использовался в Первую мировую войну как боевое отравляющее вещество.
6. Оксид серы(IV) соединение серы с кислородом состава SO₂. В нормальных условиях представляет собой бесцветный газ с характерным резким запахом (запах загорающейся спички). Тяжелее воздуха. Токсичен.SO2 очень токсичен. Симптомы при отравлении сернистым газом — насморк, кашель, охриплость, сильное першение в горле и своеобразный привкус. При вдыхании сернистого газа более высокой концентрации — удушье, расстройство речи, затруднение глотания, рвота, возможен острый отёк лёгких. При окислении образует серный газ SO₃, КОТОРЫЙ ИДЕТ НА ПРОИЗВОДСТВО СЕРНОЙ КИСЛОТЫ.
7. Ртуть Hg Ртуть при комнатной температуре представляющий собой тяжёлую серебристо-белую жидкость, пары которой чрезвычайно ядовиты. По классу опасности ртуть относится к первому классу Плотность ртути при нормальных условиях — 13 546 кг/м³.
Ртуть сохраняется в ртутных медицинских термометрах (один медицинский термометр содержит до 2 г ртути).
Парами ртути заполняют люминесцентные лампы, поскольку пары светятся в тлеющем разряде. Без люминофора ртутные лампы являются источником жёсткого ультрафиолета (254 нм), в каковом качестве и используются для обеззараживания помещений-Кварцевыми. Ртуть тоэтому они называются акже иногда применяется в качестве рабочего тела в тяжелонагруженных гидродинамических подшипниках.
Воздействие ртути — даже в небольших количествах — может вызывать серьёзные проблемы со здоровьем и представляет угрозу для внутриутробного развития плода и развития ребёнка на ранних стадиях жизни.