Помогите, пожалуйста
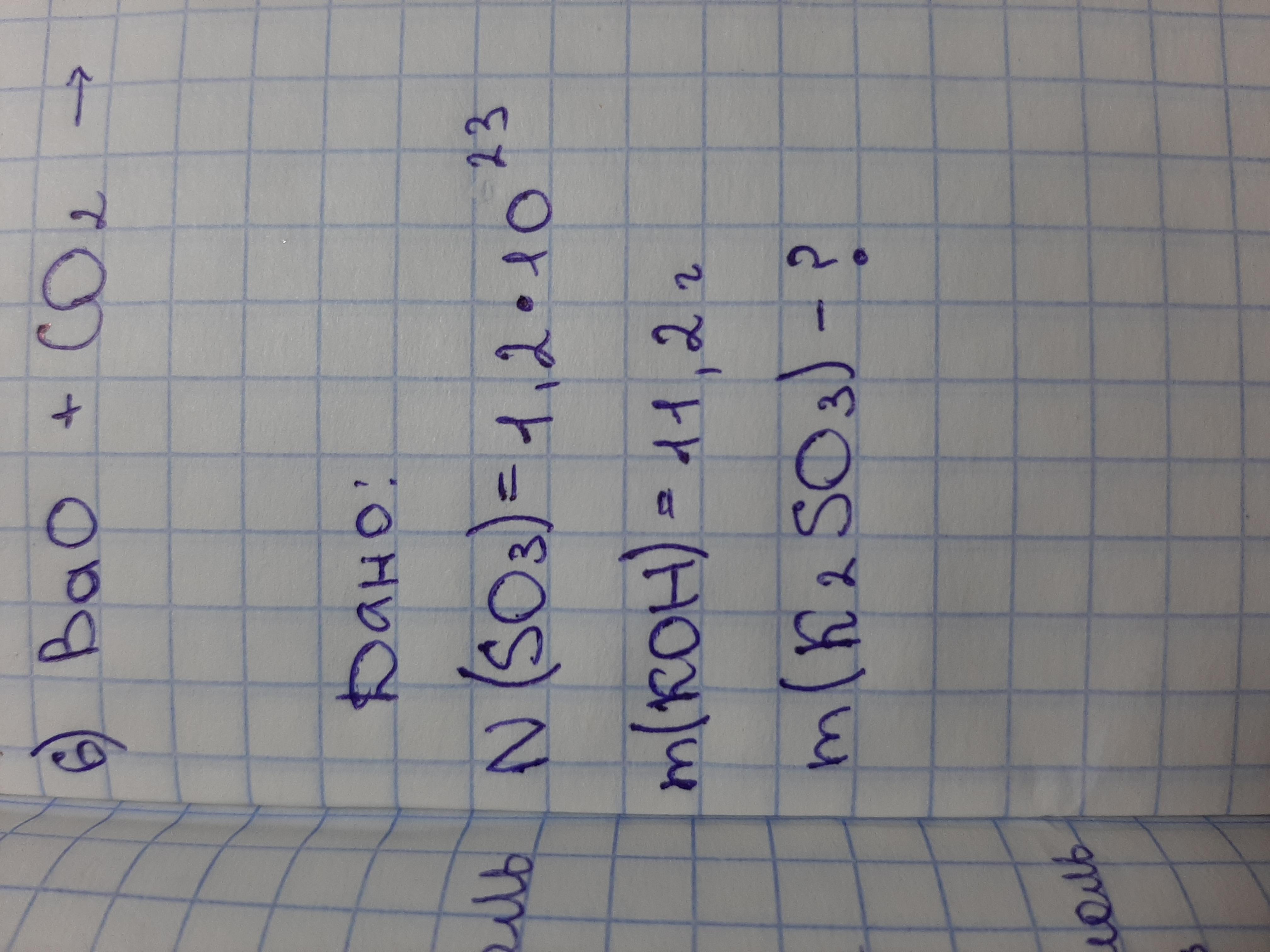
Ответы
Ответ:
m(K₂SO₄)= 17,4г.
Объяснение:
6) BaO+CO₂=BaCO₃
Задача:
N(SO₃)=1,2·10²³молекул
m(KOH)=11,2г.
Na=6,02·10²³молекул/моль
---------------------------------
m(K₂SO₄)-?
Решение:
1. Определим количество вещества оксида серы(VI) в 1,2·10²³молекул:
n₁(SO₃)=N÷Na
n₁(SO₃)= 1,2·10²³молекул÷6,02·10²³молекул/моль=0,2моль
2. Определим молярную массу гидроксида калия и его количество вещества в 11,2г.
M(KOH)=39+16+1=56г./моль
n₁(KOH)=m(KOH)÷M(KOH)=11,2г.÷56г./моль=0,2моль
3. Запишем уравнение реакции:
SO₃+2KOH=K₂SO₄+H₂O
а)по уравнению реакции:
n(SO₃)=1моль n(KOH)=2моль
б) по условию задачи:
n₁(SO₃)=0,2моль n(KOH)=0,2моль
Делаем вывод, что оксида серы(VI) находится в избытке.
Дальше задачу решаем используя количество вещества гидроксида калия:
а)по уравнению реакции:
n(KOH)=2моль n(K₂SO₄)=1моль
б) по условию задачи:
n(KOH)=0,2моль n₁(K₂SO₄)=0,1моль
4. Определим молярную массу сульфата калия и его массу количеством вещества 0,1моль:
M(K₂SO₄)=2x39+32+4x16=174г./моль
m(K₂SO₄)= n₁(K₂SO₄)×M(K₂SO₄)=0,1моль×174г./моль=17,4г.
5. Ответ: при взаимодействии оксида серы(VI) числом молекул 1,2·10²³ с гидроксидом калия массой 11,2г., образуется сульфат калия массой 17,4г.