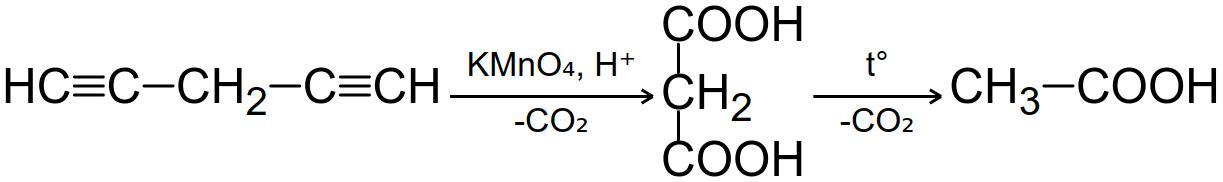Неизвестное органическое вещество массой 10,24 г сожгли в кислороде, при этом образовалось 17,92 л углекислого газа (при н.у.) и 5,76 г воды. Относительная плотность паров данного вещества по воздуху составляет 2,207. Известно, что при взаимодействии этого вещества с горячим подкисленным раствором перманганата калия образуется соединение, термическое разложение которого приводит к образованию одноосновной карбоновой кислоты и углекислого газа.
Ответы
Ответ:
C₅H₄ (пентадиин-1,4)
Объяснение:
Пишем схему горения предполагая наличие кислорода
Считаем количество вещества углекислого газа
n(CO₂) = n(C) = V(CO₂) / Vm = 17.92 / 22.4 = 0.8 моль
Считаем количество вещества воды
n(H₂O) = ½n(H) = m(H₂O) / M(H₂O) = 5.76 / 18 = 0.32 моль
Считаем сумму масс углерода и водорода
m(C, H) = M(C) * n(C) + M(H) * n(H) = 12 * 0.8 + 1 * 0.64 = 10.24 г
Значит вещество не содержит кислород, поэтому схема
Выведем эмпирическую формулу углеводорода
n(C) : n(H) = 0.8 : 0.64 = 1.25 : 1 = 5 : 4 (C₅H₄) М = 64 г/моль
Считаем молекулярную массу углеводорода
M(CxHy) = D * M(возд.) = 2.207 * 29 = 64 г/моль
Значит эмпирическая формула является истинной
Ну и приведем еще схемы реакций из которых стает понятна структурная формула этого углеводорода (см. рис.)